(14分)某溶液中可能含Mg2+、Al3+、Fe3+、Cu2+、NH4+、K+中的几种离子。当加入过量的过氧化钠时,有无色无味的气体产生,同时生成白色沉淀。加入的过氧化钠的量与产生沉淀的量之间的关系如图所示,试回答: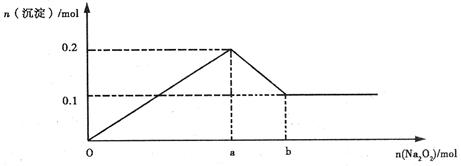
(1)该溶液中一定有 离子,一定没有 离子。
(2)无法确定是否含有 离子。要确定是否存在该离子,还需做 实验,存在该离子的实验现象为 。
(3)线段oa:ab=
短周期的四种元素W、X、Y、Z,原子序数依次变小,四种元素的原子核外电子层数之和为8。X元素的原子最外层电子数等于Y和Z两元素的原子最外层电子数之和。W元素和Y元素的原子最外层上的电子数分别是各自电子层数的2倍。X和Z可以形成XZ3的化合物。
(1)(XZ4)2W属于离子化合物,写出此化合物的化学式_________________。
(2)在A物质的一个分子里含有一个W原子,一个X原子,一个Y原子和一个Z原子,四个原子共形成5对共用电子对,写出此分子的结构式_______________。A物质生成的钾盐溶液常用检验___________(填写一种阳离子符号)。
下表中的数据是破坏1mol物质中的化学键所消耗的能量(kJ):
| 物质 |
Cl2 |
Br2 |
I2 |
HCl |
HBr |
HI |
H2 |
| 能量(kJ) |
243 |
193 |
151 |
432 |
366 |
298 |
436 |
根据上述数据回答下列问题:
(1)下列物质本身具有的能量最低的是。
A.H2B.Cl2 C.Br2 D.I2
(2)X2+H2 2HX (X代表Cl、Br、I)的反应是放热反应还是吸热反应?
2HX (X代表Cl、Br、I)的反应是放热反应还是吸热反应?
(3)相同条件下,X2 (X代表Cl、Br、I)分别与氢气反应,当消耗等物质的量的氢气时,放出或吸收的热量最多的是。
(4)若无上表中的数据,你能回答问题(3)吗?(回答“能”或“不能”)。你的依据是。
经验表明,除氢和氦外,当元素原子的电子层数(n)多于或等于原子最外层电子数(m)时,该元素属于金属元素;当元素原子的最外层电子数(m)多于电子层数(n)时,该元素属于非金属元素,其数学表达式为n≥2;(n-m)≥0时是金属元素;(n-m)<0时是非金属元素。试回答以下问题:
(1)第n周期有种主族金属元素。有种非金属元素。
(2)第m主族有种非金属元素。
(3)根据以上规则,预言未来发现的第七周期元素中,有种非金属元素,其理由是。
在某体积为2L的密闭容器中充入1.5mol NO2和2mol CO,在一定条件下发生反应: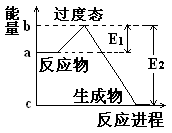
NO2+CO CO2+NO,2 min时,测得容器中NO的物质的量为0.5 mol ,则:
CO2+NO,2 min时,测得容器中NO的物质的量为0.5 mol ,则:
(1)此段时间内,用CO2表示的平均反应速率为。
(2)2 min时,容器内气体的总物质的量为。
(3)假设此反应在5 min时达到平衡,则此时容器内气体的总物质的量(填“大于”、“小于”或“等于”)2 min时容器内气体的总物质的量。
原电池是一种________________________装置。电子表所用的某种钮扣电池的电极材料为Zn和Ag2O,电解质溶液为KOH,其电极反应式为:
Zn+2OH--2e-=ZnO+H2O Ag2O+H2O+2e-=2Ag+2OH-
电池的负极是____________,正极发生的是____________反应(填反应类型),总反应式为___________________________________。