下列说法正确的是
| A.常温下,将pH=3的醋酸溶液加水稀释到原体积的10倍后,溶液的pH=4 |
| B.为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH。若pH>7,则H2A是弱 酸;若pH<7,则H2A是强酸 |
| C.用0.2000 mol∙L−1 NaOH标准溶液滴定HCl与CH3COOH的混合溶液(混合液中两种酸的浓度均约为0.1 mol∙L−1),至中性时,溶液中的酸未被完全中和 |
| D.相同温度下,将足量AgCl固体分别放入相同体积的①蒸馏水、②0.1mol/L盐酸、③0.1 mol/L氯化镁溶液、④0.1mol/L硝酸银溶液中,Ag+浓度:①>④=②>③ |
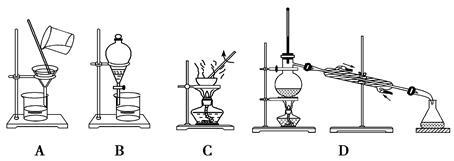
现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液 ⑧氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是
| A.分液、蒸馏、萃取 | B.萃取、蒸馏、分液 |
| C.分液、萃取、蒸馏 | D.蒸馏、萃取、分液 |
下表各组物质分类不正确的是
| A |
B |
C |
D |
|
| 液氧、空气 、Cl2 、铜丝 |
HCl、H2SO4、H2O 、HNO3 |
NaCl溶液、盐酸、CuSO4•5H2O |
NH3、NaOH 、BaSO4固体 |
|
| 分类标准 |
单质 |
酸 |
混合物 |
电解质 |
| 不属于该类的物质 |
空气 |
H2O |
盐酸 |
NH3 |
胶体区别于其他分散系的本质特征是
| A.胶体的分散质能通过滤纸空隙,而浊液的分散质不能 |
| B.胶体能产生丁达尔现象 |
| C.胶体分散质粒子直径在1nm~100nm之间 |
| D.胶体在一定条件下能稳定存在 |
下列有关氧化还原反应的叙述正确的是
| A.肯定有一种元素被氧化,另一种元素被还原 |
| B.在反应中应有沉淀、气体或水生成 |
| C.置换反应一定属于氧化还原反应 |
| D.化合反应和复分解反应有可能是氧化还原反应 |
如果你家里的食用花生油不小心混入了大量的水,利用你所学的知识,最简便的分离方法是