下图所示的是一些常见的单质、化合物之间的转化关系图,有些反应中的部分物质和反应条件被略去。常温常压下,化合物A是家庭生活中常用的一种调味品,A、C的焰色反应都呈黄色,B是无色无味的液体,D是黄绿色气体,E、F都是无色气体,F的水溶液是盐酸,H的水溶液具有漂白、杀菌性,J在水溶液中生成时为红褐色沉淀。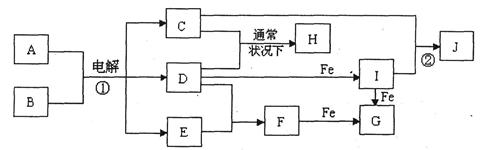
(1)H的化学式为 。
(2)F的电子式为 。
(3)反应①的化学方程式为 。
(4)反应②的离子方程式为 。
室温时10 mL某气态烃与过量的氧气混合,完全燃烧后的产物通过浓硫酸,再恢复到至室温,气体体积减少了35 mL ,剩余气体再通过氢氧化钠溶液,体积又减少了40 mL 。求气态烃的分子式并写出该分子式的同分异构体。
如右图所示,已知A的产量是一个国家石油化工水平的标志,D具有酸性。E是具有香味的不溶于水的液体。
(1)写出A分子的空间构型是:,结构简式
(2)写出A→B的化学反应方程式:
,反应类型为:。
(3)写出B→C的化学反应方程式:
,反应类型为:。
A、B、C为短周期元素,在周期表中所处的位置如图所示,A、C两元素的原子核外电子数之和等于B原子的质子数,B原子核内质子数和中子数相等。
(1)写出A、B、C三种元素的名称、、。
(2)B元素位于元素周期表中第周期,第族。
(3)C的原子结构示意图为,C的氢化物的电子式。
(4)由元素A、C及氢元素形成的化合物(AH4C)中含有的化学键的类型有。
(1)埋在地下的输油铁管道,在下列情况下,①在含铁元素较多的酸性土壤中、②在潮湿疏松透气的土壤中、③在干燥致密不透气的土壤中、④在含碳颗粒较多,潮湿透气的中性土壤中。被腐蚀速率最慢的是
(2)以石墨棒为两极,氯化铜溶液为电解液组成的电解池的
阴极电极反应式是
在化学反应中发生的能量转变形式是
运用比较方法是化学科学中研究物质性质的基本方法之一,请运用比较法解答下题:过氧化钠几乎可与所有的常见气态非金属氧化物反应。
如:2Na2O2+2CO2=2Na2CO3+O2↑,Na2O2+2CO=Na2CO3。
(1)试分别写出Na2O2与SO2、SO3反应的化学方程式:
。
。
(2)通过比较可知,当非金属元素处于价时,其氧化物与过氧化钠
反应有O2生成。