下图两个装置中,液体体积均为200 mL,开始工作前电解质溶液的浓度均为0.5 mol/L,工作一段时间后,测得有0.02 mol电子通过,若忽略溶液体积的变化
下列叙述正确的是
| A.产生气体体积 ①=② |
| B.①中阴极质量增加,②中正极质量减小 |
| C.溶液的pH变化:①减小,②增大 |
| D.电极反应式:①中阳极:4OH- - 4e- = 2H2O+O2↑ ②中负极:2H++2e-=H2↑ |
向一定量的Fe、FeO、Fe2O3的混合物中加入100 mL 1 mol/L的盐酸,恰好使混合物完全溶解,放出224 mL(标准状况)的气体,所得溶液中加入KSCN溶液无红色出现,若用足量的CO在高温下还原相同质量的此混合物,能得到的铁的质量为
| A.11.2 g | B.5.6 g | C.2.8 g | D.无法计算 |
新鲜水果、蔬菜、乳制品中富含的维生素C具有明显的抗衰老作用,但易被空气氧化。某课外小组利用碘滴定法测某橙汁中维生素C的含量,其化学方程式如下,下列说法正确的是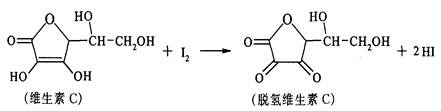
| A.上述反应为取代反应 | B.维生素C能抗衰老是因为有氧化性 |
| C.滴定时可用淀粉溶液作指示剂 | D.维生素C能发生银镜反应 |
将某些化学知识用数轴表示,具有直观形象、简明易记的优点。下列用数轴表示的化学知识中不正确的是
A.分散系的分类: |
B.AlCl3和NaOH溶液反应后产物中铝元素的存在形式: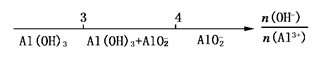 |
C.常温下甲基橙的变色范围: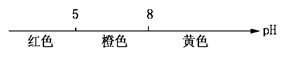 |
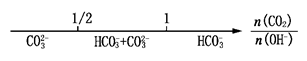
| D.CO2与NaOH溶液反应的产物: |
某硫酸镁和硫酸铝的混合溶液中,c(Mg2+ )=2 mol·L-1,c(SO42-)=6.5 mol·L-1,若将200 mL此混合液中的Mg2+和Al3+分离,至少应加入1.6 mol·L-1氢氧化钠溶液的体积是
| A.0.5 L | B.1.625 L | C.1.8 L | D.2 L |
中药狼把草的成分之一M具有清炎杀菌作用,M的结构如图所示:下列叙述正确的是 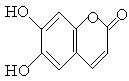
| A.M的相对分子质量是180 |
| B.1 mol M最多能与2molBr2发生反应 |
| C.M与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H4O5Na4 |
| D.1mol M与足量NaHCO3反应能生成2 mol CO2 |