亚硝酸钠(NaNO2)是一种外观与食盐相似的食品添加剂。某化学兴趣小组进行如下实验。
【实验I】
用如下装置(已省略夹持装置)制NaNO2。
已知:2NO+Na2O2=2NaNO2;2NO2+Na2O2=2NaNO3。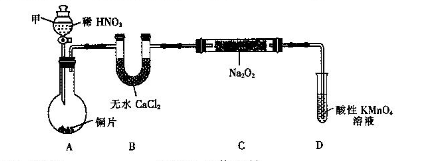
(1)仪器甲的名称是________.装置B的作用是_________________________。
(2)装置D可将剩余的NO氧化成NO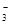 ,发生反应的离子方程式为_____________。
,发生反应的离子方程式为_____________。
(3)使用气密性良好的上述装置进行实验,NaNO2的纯度较低。为提高NaNO2纯度须对上述实验装置或药品进行改进,其改进措施是________________________________。
【实验Ⅱ】
利用目视比色法(比较溶液颜色深浅以测定物质浓度)测定泡菜样品中NaNO2的含量。
步骤i:在5个有编号的试管中分别加入不同量的NaNO2溶液,各加入1 mL的M溶液(M遇NaNO2呈紫红色,NaNO2浓度越大颜色越深),再加蒸馏水至总体积均为l0 mL并振荡,制成标准色阶。

步骤ⅲ:取5 mL待测液X,加入1 mLM溶液,加蒸馏水至10mL振荡,与标准色阶比较。
(4)步骤ii获取待测液X的过程中,加入明矾的目的是__________。
(5)步骤iii比较结果与④号色阶颜色相同,此泡菜样品中NaNO2的含量为_________mg·kg-1
(6)用目视比色法证明泡菜中加入维生素C可以降低NaNO2的含量。设计并完成下列实
验报告。
在一定条件下,二氧化硫和氧气发生如下反应:2SO2(g)+ O2 (g)  2SO3(g) △H< 0。查阅资料知SO3熔点16.83℃,沸点44.8℃。
2SO3(g) △H< 0。查阅资料知SO3熔点16.83℃,沸点44.8℃。
(1)600℃时,在一密闭容器中,将二氧化硫和氧气混合,反应过程中SO2,O2,SO3物质的量变化如图。
①该反应的化学平衡常数表达式 K=
②该反应能自发进行的原因是。
③据图判断,该反应处于平衡状态的时间是。
④据图判断,反应进行至20 min时,曲线发生变化的原因是(用文字表达)。
(2)某化学研究学习小组用下图的装置组装设计了一个实验,以测定SO2转化为SO3的转化率,仪器的连接顺序是a→h→i→b→c→f→g→d→e。
①为提高SO2的转化率,实验时Ⅰ处滴入浓硫酸与Ⅱ处加热催化剂的先后顺序是。
②在Ⅰ处用大火加热烧瓶时SO2的转化率会。(填“填大”“不变”或“减小”)
③用n mol Na2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,称得Ⅲ处增重 m g,则本实验中SO2的转化率为。
用一定物质的量浓度的NaOH溶液滴定10.00 mL已知浓度的盐酸,滴定结果如图所示。回答下列问题:
(1)有关滴定的操作可分解为如下几步,并补充完整。①用NaOH溶液润洗滴定管。②取NaOH溶液注入碱式滴定管至“0”刻度以上2~3 mL。③④调节液面至“0”或“0”刻度以下,记下读数。⑤移取10.00 mL盐酸注入锥形瓶中,加入酚酞。⑥把锥形瓶放在滴定管的下面,用氢氧化钠溶液滴定并记下读数。
(2)若滴定前俯视滴定管读数,滴定后平视刻度读数,则会使氢氧化钠浓度的测定结果(填“偏高”“偏低”或“不变”)。
(3)如用酚酞作指示剂,则滴定终点的实验现象是。
(4)c(HCl)=mol·L-1
(5)c(NaOH) =mol·L-1
(6)右图表示50 mL滴定管中液面的位置,如果液面处的读数是a ,则滴定管中液体的体积(填代号)。
| A.是a mL | B.是(50-a)mL |
| C.一定大于a mL | D.一定大于(50-a)mL |
(7)常温下,用0.01 mol•L-1H2SO4溶液滴定0.01 mol•L-1 NaOH溶液,中和后加水至100 ml。若滴定到终点时少加一滴H2SO4(设1滴为0.05 ml)。则此时溶液的pH为。
某同学用如图一所示装置来探究CO2、SO2与澄清石灰水的反应,结果通入CO2可以看到先浑浊后澄清的现象,但通入SO2没有看到浑浊现象。经过思考分析后,该同学改用图二的装置,将气体收集在注射器,缓缓地将气体一个气泡一个气泡地通入澄清石灰水中,都能看到石灰水先变浑浊再澄清的现象。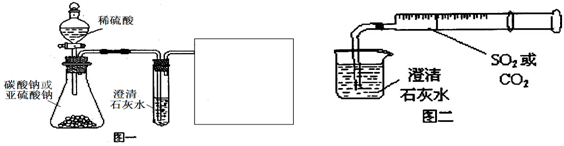
(1)SO2是空气污染物之一,它的危害是。
(2)图一中生成CO2反应的离子方程式为;
(3)如何鉴别CO2和SO2(只需要写出一种方法,应写出操作方法、现象和结论)?。
(4)用图一进行SO2与石灰水反应的实验时,从环保角度考虑,还需要增加什么装置,在方框中画出。
(5)对比分析两组实验,你认为用图一装置实验时,通过SO2不能出现浑浊的原因可能是。
下表是某兴趣小组通过实验获得的相同体积足量稀硫酸与铁反应的实验数据:
| 实验序号 |
金属质量/g |
金属状态 |
c(H2SO4) mol/L |
实验温度/℃ |
金属消失的时间/s |
|
| 1 |
0.10 |
丝 |
0.7 |
20 |
250 |
|
| 2 |
0.10 |
丝 |
1.0 |
20 |
200 |
|
| 3 |
0.10 |
粉末 |
1.0 |
20 |
125 |
|
| 4 |
0.10 |
粉末 |
1.0 |
30 |
50 |
分析上述数据,回答下列问题:
(1)反应的离子方程式:。
(2)①实验1、2可得出的结论是;
②实验2、3可得出的结论是;
③实验3、4可得出的结论是。
.(12分)某铝合金(硬铝)中含有镁、铜、硅,为了测定该合金中铝的含量,某同学设计如下试验:
(1)取样品 ag ,称取时使用的仪器名称为。
(2)将样品溶于足量的稀盐酸中,过滤,滤渣中含有,在溶解过滤时使用的玻璃仪
器有。
(3)往滤液中加入过量的NaOH溶液、过滤,写出该步操作中有关的离子方程式。
(4)在第( 3 )步的滤液中通入足量CO2,过滤。有关反应的离子方程式是。
(5)步骤(4)过滤后的滤渣用蒸馏水洗涤数次后,烘干并灼烧至质量不再减轻为止,冷却后称量,质量为bg,则原样品中铝的质量分数是。
(6)若步骤(3)中加入氢氧化钠的量不足,则实验结果偏(填“高”、“低”或“不影响”,下同);若步骤(5)中滤渣没有洗涤,则实验结果偏;若滤渣燃烧不充分,则实验结果偏。