下图表示的是向Na2CO3溶液中滴入稀盐酸时产生CO2的过程。
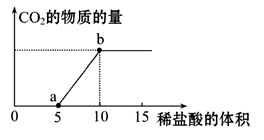
(1)写出a点以前发生反应的离子方程式:
(2)写出a到b点发生反应的离子方程式:
(3)若某Na2CO3溶液中含n mol Na2CO3,向其中滴入一定量的稀盐酸,恰好使溶液中Cl-和HCO3-的物质的量之比为2∶1,则滴入的稀盐酸中的HCl的物质的量为 mol(用含n的代数式表示)。
(14分)实验题:某班级的探究小组研究氧化铜能否在氯酸钾的受热分解中起到催化剂的作用,设计了如下实验:
(一)制备氧化铜
(1)称取5.0g CuSO4·5H2O晶体,研细后溶解:此步骤需要的仪器有________________________。
(2)向盛有硫酸铜溶液的烧杯中滴加NaOH溶液,直到不再产生沉淀为止。此步实验现象:____________;离子方程式为:_________________。
(3)A.把步骤(2)中的溶液和沉淀转移到蒸发皿内,稍微加热至沸腾,搅拌,直到沉淀全部变为黑色固体,停止加热,再过滤、洗涤、干燥、再转移到研钵中研细备用。
B.把步骤(2)中的溶液和沉淀转移到过滤器中过滤,洗涤,将上述沉淀在蒸发皿中进行蒸发,至全部变为黑色固体为止。再转移到研钵中研细备用。
你认为那一个步骤更好,说明理由:______________________。
(二)证明氧化铜起催化剂作用
设计对比实验①任取两份氯酸钾,分别放入两支试管,在其中一份中加入经精确称量的ng氧化铜粉末;②将两份氯酸钾同时在相同条件下正确加热,将放出的气体通入水中;③停止加热,冷却,将原先混有氧化铜的反应后混合物加水溶解,小心过滤,得到滤出物,洗涤并干燥;④观察滤出物的颜色和状态;⑤将滤出物和炭粉混和,在密闭容器中高温加热,将反应产生的气体通入澄清的石灰水中,并观察试验现象。
请回答下列问题:
(1)氧化铜作催化剂的理论依据是:_____________________。
(2)以上实验步骤,有一步不够严密,请指出是那一步:______(填步骤序号);该步骤应该做何改进?__________________。
(3)要达到实验目的,还应该再增加一个实验步骤,这个实验步骤是______。
(4)若用另一套实验装置和操作替换第⑤步实验,也可以达到这一步的实验目的,请从图中所给的仪器作出合理选择,将它们连接成一个符合设计者要求的试验装置。
这个实验装置按照气流从左到右的连接顺序是__接__接__接__接__接__。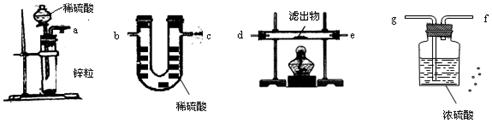
下列框图中的A ~ K物质均为中学常见物质。已知B、D、E、L常温下为密度比空气大的气体,D、E为单质,其它为化合物。A和I都是常用的漂白剂,F的焰色反应呈黄色。F、G均能与L的水溶液反应放出B。请根据图示关系回答问题: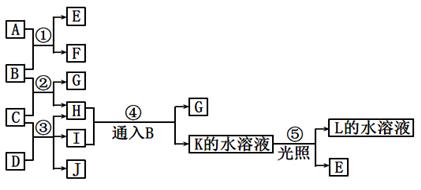
(1)F的俗名是______;K的电子式______。
(2)反应①~⑤中,属于氧化-还原反应的是______。
(3)反应④的离子方程式________________________。
反应③的化学方程式________________________。
(4)某单质能与H反应生成E,该反应的化学方程式为____________。
2005年10月5日,瑞典皇家科学院将本年度诺贝尔化学奖授予法国化学家伊夫·肖万和两位美国化学家罗伯特·格拉布和理查德·施罗克,以表彰他们在烯烃复分解反应研究和应用方面做出的卓越贡献。


伊夫·肖万罗伯特·格拉布理查德·施罗克
烯烃复分解反应实际上是在金属烯烃络合物的催化下实现C=C双键两边基团换位的反应。如下图表示了两个丙烯分子进行烯烃换位,生成两个新的烯烃分子——2-丁烯和乙烯:
现以石油裂解得到的丙烯为原料,经过下列反应可以分别合成重要的化工原料I和G。I和G在不同条件下反应可生成多种化工产品,如环酯J。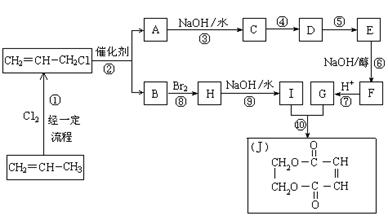
请按要求填空:
(1)写出下列反应的反应类型:
③:,⑥:,⑧:。
(2)反应②的化学方程式是:。
(3)反应④、⑤中有一反应是与HCl加成,该反应是(填反应编号),设计这一步反应的目的是;物质E的结构简式是。
(4)反应⑩的化学方程式是。
A、B、C、D、E、F六种元素均是短周期元素,且原子序数依次增大。B、F原子的最外层电子数均为其电子层数的两倍,D、F元素原子的最外层电子数相等。X、Y、Z、W、甲、乙六种物质均由上述元素的两种或三种元素组成,元素B形成的单质M与甲、乙均能反应(相对分子质量甲<乙)转化关系如图(反应条件略去),元素E形成的单质是 “21世纪的能源”,是目前应用最多的半导体材料。请回答下列问题: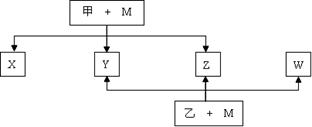
(1)写出M与甲的浓溶液加热时反应的化学方程式。
(2)X、Y、Z、W属于同一类物质,这类化合物固态时的晶体类型为;X、Y、W都能与Z反应,则Z的结构式为。
(3)将X、W与D2按1∶1∶n的物质的量之比通入Z中,充分反应后无气体剩余或生成,则n=,写出反应的化学方程式。
(4)化合物ED2与元素B形成的某种单质晶体类型相同,且在高温下能发生置换反应。若反应中B的单质被破坏1 mol共价键,则参加反应的化合物ED2的质量为g。
(5)元素B的另一种单质具有平面层状结构,同一层中的原子构成许许多多的正六边形,则12 g该晶体中含有NA个正六边形。
TiO2在工业生产和日常生活中有重要用途。
I.工业上用钛矿石(FeTiO3,含FeO、Al2O3、SiO2等杂质)经过下述反应制得:
其中,步骤②发生的反应为:2H2SO4+FeTiO3=TiOSO4+FeSO4+2H2O。
(1)净化钛矿石时,是否需要除去杂质FeO?答:(填“需要”或“不需要”)。
(2)净化钛矿石时,需用浓氢氧化钠溶液来处理,写出该过程中发生反应的化学方程式。
答:。
II.TiO2可通过下述两种方法制备金属钛:
“方法一”是电解TiO2来获得Ti(同时产生O2):将处理过的TiO2作阴极,石墨为阳极,熔融CaCl2为电解液,用碳块作电解槽池。
(3)阴极反应的电极反应式为___________________________________。
(4)电解过程中需定期向电解槽池中加入碳块的原因是______________________。
“方法二”是先将TiO2与Cl2、C反应得到TiCl4,再用镁还原得到Ti。因下述反应难于发生:
TiO2 (s)+2Cl2 (g) TiCl4(l)+O2 (g)ΔH=+151 kJ·mol-1
TiCl4(l)+O2 (g)ΔH=+151 kJ·mol-1
所以不能直接由TiO2 和Cl2反应(即氯化反应)来制取TiCl4。当往氯化反应体系中加入碳后,碳与上述反应发生耦合,使得反应在高温条件下能顺利进行。
(5)已知:C(s)+O2 (g) = CO2 (g)ΔH=-394 kJ·mol-1。请填空:
TiO2 (s)+C (s)+2Cl2 (g) = TiCl4 (l)+CO2 (g)ΔH= ______________
(6)从化学平衡的角度解释:往氯化反应体系中加入碳时,氯化反应能顺利进行的原因。
答:____________________________________________。