化学是一门以实验为基础的科学,请结合图示回答问题: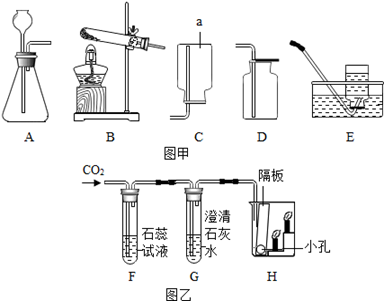
(1)写出仪器a的名称 ;
(2)实验室中制取CO2的药品为 和 (填名称),反应的化学方程式为:
收集装置是 (填字母)
(3)小彭同学设计了如图乙装置并验证二氧化碳的性质,当通入二氧化碳一段时间后,F中的现象是 ;G中澄清石灰水变浑浊,反应的化学方程式为 H中观察到蜡烛由低到高依次熄灭,说明
自来水的生产过程主要有下列几步净化水的方法①过滤②吸附沉淀③静置沉淀④活性炭吸附⑤加药物杀菌清毒,在自来水的生产时上述的先后顺序为(填序号),其中发生了化学变化的是(填序号),自来水仍是硬水,最简单鉴别硬水和软水的方法是向水中加入,若产生现象则是硬水。
实验室用加热氯酸钾和二氧化锰的混合物制氧气,当氯酸钾全部分解完后停止加热,现要将试管内的难溶性二氧化锰从试管内的残余物中分离出来,先将混合物溶于水,再用法分离,在该操作中玻璃棒的作用是,若在该实验后得到母液仍较浑浊,其原因有①;
②。
有下列物质①稀硫酸②自来水③液态氮④氯酸钾晶体⑤二氧化锰⑥硫磺,其中属于混合物的有(填序号),属于单质的有,是氧化物的有。
指出下列数字或符号的意义:
SO2 ①②
4Ca2+
按要求写出下列合适的化学用语:
二个氮原子 二个硫离子二个氧分子
一个镁离子 氢氧根离子铵根离子