根据下列几种粒子的结构示意图,回答问题:(填粒子代号)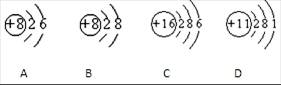
(1)其中属于阴离子的是 ,
(2)属于金属元素的是 ,
(3)具有相似化学性质的是 。
实验题:
I.海藻中提取碘的流程如图,已知②中发生反应的化学方程式为:
Cl2+2KI===2KCl+I2。请回答下列问题:
(1)指出提取碘的过程中有关实验操作①、③的名称:________;________。
(2)在3mL碘水中,加入1mL四氯化碳,振荡、静置后,观察到试管里的分层现象是________。(注:如图试管中深色区为紫红色溶液)
(3)从含碘的有机溶液中提取碘和回收有机溶剂,还需经过蒸馏,指出如图实验装置中的错误之处。(加热装置烧杯下已垫石棉网)
①________________________________________________;
②________________________________________________。
II.某化学兴趣小组在课外活动中,对某溶液进行了多次检测,其中三次检测结果如下表所示,请回答:
| 检测次数 |
溶液中检测出的物质 |
| 第一次 |
KCl、K2SO4、Na2CO3、NaCl |
| 第二次 |
KCl、BaCl2、Na2SO4、K2CO3 |
| 第三次 |
Na2SO4、KCl、K2CO3、NaCl |
(1)三次检测结果中第________次检测结果肯定不正确。
(2)在检测时,为了确定溶液中是否存在硫酸根离子、碳酸根离子和氯离子:
第一步:向溶液中滴加过量的①________溶液(填化学式),其目的是检验CO32-并将其除去;
第二步:加入②________溶液(填化学式),其目的是③_________________________
________________________________________________________________________;
第三步:过滤,再向滤液中加入④________溶液(填化学式),其目的是⑤________________。
实验题:现需要90 mL 1.00 mol·L-1 NaCl溶液,某同学按下列步骤进行配制:
①计算所需NaCl固体的质量;
②称量NaCl固体;
③将称好的NaCl固体放入烧杯中,用适量蒸馏水溶解;
④将烧杯中的溶液注入容量瓶,并用少量蒸馏水洗涤烧杯内壁2~3次,洗涤液也注入容量瓶;
⑤向容量瓶中加蒸馏水至刻度线。
请回答有关问题:
(1)计算所需NaCl固体的质量______g。
(2)为了加速溶解,可以采取的措施是_______________。
(3)使用容量瓶的规格是________mL。
(4)如果将烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外,最后配成的溶液中溶质的实际浓度比所要求______________(填“大”或“小”)了。
(5)如果某同学是用托盘天平称量NaCl固体,那么称量的质量是 ,与计算量一致吗?解释原因___________________________。
填空题
I.如图为一“铁链”图案,小明在图案上分别写了H2、CO2、Na2O、NaCl、FeCl3五种物质,图中相连的两种物质均可归属为一类,相交部分A、B、C、D为其相应的分类依据代号。
请回答下列问题:
(1)请将分类依据代号填入相应的括号内:
①()两种物质都是钠的化合物
②( )两种物质都是氧化物
③()两种物质都是盐
④用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入饱和的上图中某种物质M的水溶液,继续煮沸可制得一种红褐色胶体。
物质M的化学式为________,写出相应的化学方程式: 。
⑤丁达尔效应是区分胶体与溶液的一种最常用的方法。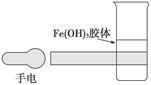
如图是在实验室中进行氢氧化铁胶体丁达尔效应实验的示意图,该图中有一处明显错误是____________________,原因是_________________(试从分散系的分类进行讨论说明)。
II.某同学拟用氯化钙固体、碳酸钠溶液和稀硝酸等试剂,先制得碳酸钙,最终制得纯净的硝酸钙晶体。
(1)写出制取过程中反应的化学方程式:_____________,______________。
(2)请帮助该同学完成下列实验操作步骤(不要求回答使用的仪器)。
①用蒸馏水完全溶解CaCl2后,加入______________________;
②将反应后的混合物过滤,并用适量蒸馏水洗涤沉淀至无Cl-;
加入_________________,使沉淀完全溶解;
③_________________,得到纯净的硝酸钙晶体。
被誉为“太空金属”的钛(Ti),在自然界中主要以金红石(TiO2)的形式存在.由于金红石熔点高,为金属Ti的直接制备带来了困难.在工业上常常采用将其先转化成熔沸点较低的TiCl4后再进行还原的方法.金红石转化成TiCl4的反应方程式如下:
TiO2 + 2C + 2Cl2═ TiCl4 + 2CO
(1)用双线桥法标出上述化学方程式的电子转移情况;
(2)指出该反应的氧化剂 ,氧化产物 ;
(3)当消耗标准状况下Cl2 11.2L时,则转移的电子数为 。
有X、Y、Z三种元素,X原子核内无中子,Y原子的核外有三层电子层,单质在常温常压下是黄绿色气体,Z原子在反应中容易失去一个电子形成稳定的结构 ,和氖具有相同的电子数。按要求回答下列问题:
(1)依次写出X、Z的元素符号: 、 ,画出Y原子结构示意图: 。
(2)元素X、Z形成的化合物与水反应有无色气体产生,反应后的溶液能使酚酞试液变红色,请写出该反应的化学方程式 。