(本题共12分)某化学小组的同学模拟工业制硝酸设计了如下图所示的装置。已知:
CaCl2+ nH2O→CaCl2·nH2O;CaCl2+ 8NH3→[Ca(NH3)8]Cl2
根据题意完成下列填空: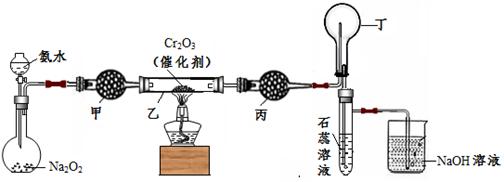
33.分液漏斗中氨水的浓度为9.0mol/L。现用质量分数为0.35、密度为0.88g/cm3的氨水配制9.0mol/L的氨水100mL,需要的定量仪器有 (选填编号)。
a.100mL容量瓶 b.10mL量筒 c.50mL量筒 d.电子天平
34.受热时,乙中反应的化学方程式为 。
35.实验开始先加热催化剂,当催化剂达红热时再打开分液漏斗活塞并移走酒精灯,可观察到的现象有 。
36.干燥管甲的作用是 ;丙中盛放的药品为 (选填下列编号),其目的是 。
a.浓H2SO4 b.无水CaCl2 c.碱石灰 d.无水CuSO4
37.丁中除了NO之外,还可能存在的气体有 (填写化学式)。烧杯中发生反应的化学方程式 、 。
镁在高温下与O2、N2或CO2均可以发生反应,试解决下列问题。
(1)工业通常采用电解熔融氯化镁冶炼金属镁,不以氧化镁为原料的理由是。
(2)将燃着的镁条伸入盛满CO2的集气瓶中,镁条剧烈燃烧,发出耀眼的白光,瓶内壁上有黑色物质生成,化学方程式为。
(3)由金红石(TiO2)制取单质钛(Ti),涉及到的反应步骤为
金属镁的作用为,在Ar气氛中的进行的理由是。
(4)现拟在实验室里利用空气和镁粉为原料制取少量氮化镁(Mg3N2)。已知:
Mg+H2O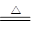 MgO+H2↑Mg3N2 +6H2O =3Mg(OH)2+2NH3↑
MgO+H2↑Mg3N2 +6H2O =3Mg(OH)2+2NH3↑
可供选择的装置和药品如下图所示。

①导管口间的连接次序是:a →( )()→()()→()()→ h
②通气后,应先点燃(填“B”或“C”)装置的酒精灯,装置A的作用是,装置E的作用是。
③请设计一个简单的小实验验证产物是氮化镁。
(1)下列实验操作或对实验事实的描述不正确的有(填序号)。
| A.用托盘天平称量17.55g氯化钠晶体 |
| B.碳酸钠溶液保存在带玻璃塞的试剂瓶 |
| C.用干燥的pH试纸测定新制氯水的pH |
| D.使用容量瓶配制溶液时,俯视刻度线定容后浓度偏大 |
E.向饱和FeCl3溶液中滴加少量NaOH溶液,可制取Fe(OH)3胶体
F.除去CO2气体中混有的少量HCl,可以将气体通入饱和碳酸氢钠溶液
(2)下图为中学化学实验中常见的实验装置


A B C
实验室常用装置A制备下表中气体,请将分液漏斗和圆底烧瓶中应装的化学试剂填写完整。
| 气体 |
O2 |
Cl2 |
NH3 |
| 分液漏斗中试剂 |
浓氨水 |
||
| 圆底烧瓶中试剂 |
KMnO4 |
可用B装置排液收集气体,气体应从该装置________(填“左”“右”)管口导进,倘若利用该装置收集Cl2,试剂瓶中盛放的试剂为。
C装置用于处理多余气体对环境的污染,若利用该装置吸收Cl2,此时烧杯中发生反应的离子方程式为。倘若该装置中仅仅盛放稀硫酸,通常不适合吸收氨气的原因是,若向烧杯中额外再加入一种液态有机物则可安全吸收氨气,这种有机物为。
测定有机物中碳和氢等元素的含量,最常用的方法是燃烧分析法。即把已知量的样品置于氧气流中,用氧化铜作催化剂,在760℃左右,样品全部被氧化为二氧化碳和水。实验装置如下图所示:
(1)实验时,装置a、b中通常装入的物质分别是、。
(2)开始加热之前,要通一段时间的氧气,目的是;停止加热后,也要通一段时间的氧气,目的是。
(3)某次实验中,取用样品烃的含氧衍生物A的质量为2.3g,经测定a装置增重2.7g,b装置增重4.4g。请推算出A物质的实验式:(要求写出计算过程)
(4)经进一步测定得知A的相对分子质量为46,则A的分子式为。
(5)实验发现A物质遇金属钠可以放出氢气,则A物质中具有的官能团为。同样取2.3g的A,与足量的钠反应,用如图所示装置量取放出的氢气。量取气体时操作水准管的注意事项为。将量取的气体换算成标准状况体积为cmL,则一个A分子中有个氢原子被置换了(用含c的表达式表示)。
二氧化硫和氯气是中学化学中的常见气体,探究二者的制法和性质是十分重要的课题。
(1)实验室可由多种途径制取SO2。
途径I:Na2SO3固体与较浓的硫酸(约70%)反应制取;
途径II:铜与浓硫酸加热制取。
如果要在实验室制取SO2,选用上述两种方法中的(填“途径I”或“途径II”)更合理,你的理由是(答出一点就可)。
(2)如图是用KMnO4与浓盐酸反应制取适量氯气的简易装置。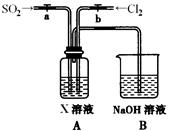
已知:2 KMnO4+16HCl(浓)= 2KCl+2MnCl2+5Cl2↑+8H2O。装置B、C、D的作用分别是:
B:;
C:;
D:。
(3)某同学设计用如下装置探究二氧化硫、氯气的化学性质。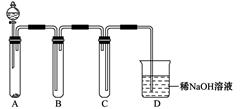
通过控制弹簧夹a、b,向装置A中分别通入不同气体,请完成如下问题:
①若关闭b,打开a,若X为品红溶液,则A中的现象为:,说明二氧化硫具有性。
②若关闭a,打开b,若X为紫色石蕊试液,则A中的现象为:,原因是。
③若同时打开a、b,且通入的气体体积比为1:1,若X为紫色石蕊试液,则A中的现象为,与②现象不同的原因是(书写相应的化学方程式)。
某研究性学习小组将一定浓度的Na2CO3溶液滴入MgSO4溶液中得到白色沉淀。甲同学认为两者反应只生成MgCO3一种沉淀;乙同学认为这两者相互促进水解,只生成Mg(OH)2一种沉淀;丙同学认为生成MgCO3和Mg(OH)2两种沉淀。(查阅资料知:MgCO3和Mg(OH)2均不带结晶水)
(1)按照乙同学的理解Na2CO3溶液和MgSO4溶液反应的化学反应方程式为___________________;
在探究沉淀物成分前,须将沉淀从溶液中分离并净化。具体操作为①过滤②洗涤③干燥。
(2)请用下图所示装置,选择合适的实验装置和必要的试剂,证明沉淀物中只有碳酸镁。
①各装置连接顺序为__________________(用装置编号表示);
②装置C中装有试剂的名称是______________;
③能证明生成物中只有MgCO3的实验现象是_______。
(3)若Mg(OH)2和MgCO3两者都有,可通过下列所示装置的连接,进行定量分析来测定其组成。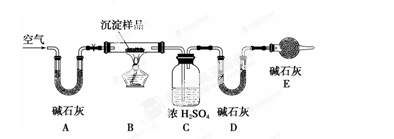
实验结束时通入过量的空气的作用是______________________________。
A装置和E装置的共同作用是__________________________。
③实验过程中测定的数据有:W1:样品的质量,W2:反应后装置B中残渣的质量,W3:反应生成水的质量,W4:反应生成二氧化碳的质量,为了测定其组成,至少需要其中____个数据,请将可能的组合填入下表中(每个空格中填一种组合)。