(本题共12分)绿矾(FeSO4·7H2O)是治疗缺铁性贫血药品中的重要成分。下面是以市售铁屑(含少量锡、氧化铁等杂质)为原料生产纯净绿矾的一种方法:
已知:室温下饱和H2S溶液的pH约为3.9;SnS沉淀完全时溶液的pH为1.6;FeS开始沉淀时溶液的pH为3.0,沉淀完全时的pH为5.5。
请回答下列问题:
(一)绿矾的制备
38.检验制得的绿矾中是否含有Fe3+的实验操作是 。
39.操作II中,通入硫化氢至饱和的目的是 ;在溶液中用硫酸酸化至pH=2的目的是 。
40.操作IV的顺序依次为: 、冷却结晶、 。
(二)绿矾中FeSO4·7H2O含量的测定
若用容量法测定绿矾中FeSO4·7H2O的含量。滴定反应是:5Fe2+ + MnO4—+8H+"5Fe3+ +Mn2++4H2O 。
实验方案如下:
① 称取15.041 g绿矾产品,溶解,在250mL容量瓶中定容。
② 量取25.00mL待测溶液于锥形瓶中。
③ 用0.0500mol/L KMnO4溶液(硫酸酸化)滴定至终点,记录初读数和末读数。
④ 。
⑤ 数据处理。
41.上述实验方案中的步骤④是 。洁净的滴定管在滴定前必须进行的操作有:
① 检验活塞是否漏水;
② ;
③ 向滴定管中加入KMnO4标准溶液到0刻度以上,赶走尖嘴部位的气泡,调节初读数。
(三)数据处理
某小组同学的实验数据记录如下:
| 实验次数 |
初读数(mL) |
末读数(mL) |
| 1 |
0.20 |
21.40 |
| 2 |
0.00 |
21.00 |
| 3 |
1.60 |
26.60 |
42.上述样品中FeSO4·7H2O的质量分数为 (用小数表示,保留三位小数)。
红矾钠(重铬酸钠:Na2Cr2O7·2H2O)是重要的基本化工原料,在印染工业、电镀工业和皮革工业中作助剂,在化学工业和制药工业中也用作氧化剂,应用领域十分广泛。
(1)实验室中红矾钠可用铬铁矿(主要成分:FeO·Cr2O3)利用以下过程来制取。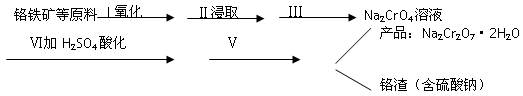
①步骤I中反应的化学方程式为: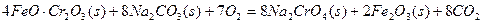 该反应的化学平衡常数的表达式为 ,在常温下该反应速度极慢,下列措施中能使反应速率增大的是 。
该反应的化学平衡常数的表达式为 ,在常温下该反应速度极慢,下列措施中能使反应速率增大的是 。
| A.升高温度 | B.通入过量的空气 | C.将原料粉碎 | D.增加纯碱的用量 |
②步骤Ⅱ中所得溶液显碱性,其中除含有Na2CrO4外还含有铝、硅元素的化合物,它们的化学式可能是 、 。
③步骤Ⅲ需将溶液的pH调至7~8并煮沸,其目的是 。
④步骤Ⅳ中发生反应的离子方程式为: 。
(2)将红矾钠与KCl固体1:2(物质的量比)混合溶于水后经适当操作可得到K2Cr2O7晶体。请填写表中空格。完成上述过程。
| 序号 |
实验步骤 |
简述实验操作(不必叙述如何组装实验装置) |
| ① |
溶解 |
将混合物放入烧杯中,加水,充分搅拌直到固体不再溶解。 |
| ② |
||
| ③ |
||
| ④ |
||
| ⑤ |
过滤、干燥 |
得到K2Cr2O7晶体 |
某化学研究性学习小组计论Fe3+和SO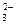 之间发生怎样的反应。可能发生的反应有:2Fe3++SO
之间发生怎样的反应。可能发生的反应有:2Fe3++SO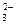 +H2O=2Fe2++SO
+H2O=2Fe2++SO +2H+(氧化还原反应)
+2H+(氧化还原反应)
2Fe3++3SO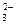 +6H2O=2Fe(OH)3(胶体)+3H2SO4(水解反应)
+6H2O=2Fe(OH)3(胶体)+3H2SO4(水解反应)
为了证明反应的实际情况,同学们设计并实施了下列实验,请填写下列空白:
实验I:学生选择的实验用品:Na2SO3浓溶液、BaCl2稀溶液、稀盐酸;试管若干、胶头滴管若干。从选择的药品分析,实验者设计这个实验的目的是
。
实验II:①取5mLFeCl3浓溶液于试管中,逐滴加入Na2SO3浓溶液,观察到溶液颜色由黄色变为红棕色,无气泡产生,无沉淀生成,继续加入Na2SO3浓溶液至过量,溶液颜色加深,最终变为红褐色。这种红褐色液体是 。向红褐色液体中逐滴加入稀盐酸至过量,可以观察到的现象是
。将溶液分成两等份,其中一份加入KSCN稀溶液,溶液变成血红色,反应的离子方程式为 。
另一份加入BaCl2稀溶液,有少量白色沉淀生成,产生该白色沉淀的离子方程式是 。
②换用稀释的FeCl3和Na2CO3溶液重复实验II。实验II、III产生的现象完全相同。由上述实验得出的结论是 。
实验III:若在FeCl3浓溶液中加入Na2CO3浓溶液,观察到红褐色沉淀并且产生无色气体,该反应的化学方程式是 。
从形式上看,Na2CO3和Na2SO3相似。但是从上述实验中可以看到,二者的水溶液与氯化铁溶液反应的现象差别很大,分析其原因可能是:
① 。
②
(14分)下面是中学化学中常用玻璃仪器组成的实验装置图(根据需要可在其中加入液体或固体)。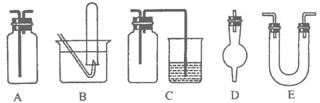
请回答下列问题:
(1)能用作干燥氨气的装置有_________(填字母);
(2)既能用于收集氯气又能用于收集一氧化氮气体的装置有_________(填字母);
(3)在氯气和铁反应实验中,能添加在制氯气和反应装置之间以除去氯气中氯化氢等杂质气体的装置有_________(填字母);
(4)能用于乙烯与溴水反应制二溴乙烷的实验装置有_________(填字母);
(5)若用C装置作二氧化硫与烧杯中氢氧化钠溶液反应的实验,则其中广口瓶的作用是_____________________________________________。
(12分)氟化钠是一种重要的氟盐,主要用作农业杀菌剂、杀虫剂、木材防腐剂。实验室可通过下图所示的流程以氟硅酸(H2SiF6)等物质为原料制取氟化钠,并得到副产品氯化铵: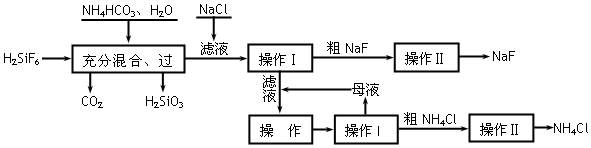
有关物质在水中溶解度分别为:
氯化铵:10℃时33.3 g、20℃时37.2 g、30℃时41.4g;氟化钠:20℃时4 g;氟硅酸钠微溶于水。
请回答下列问题:
⑴上述流程中发生两步化学反应,第一步反应的化学方程式为: ,
第二步反应能进行是因为 。
⑵操作Ⅰ需要用到的玻璃仪器除玻璃棒外,还有 。
⑶操作II的作用是 。
⑷操作Ⅲ的具体过程是 。
⑸流程中NH4HCO3必须过量,其原因是 。
为测定Na2CO3与Na2SO3混合物中各组分的含量,取样品23.2g以下图所示装置进行实验:(铁架台、铁夹等仪器未在图中画出)
(1)将仪器连接好以后,必须进行的第一步操作是___________________。
(2)此实验还必须用到的最重要的仪器是__________;仪器F的作用是________。
(3)已知仪器C中装有品红溶液,其作用是______________,有人提出该溶液可能引
起Na2CO3含量的测量结果比实际值偏低,理由是____________________。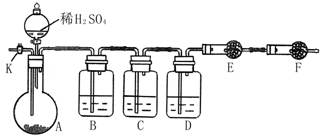
(4)实验室中备有以下常用试剂:
a.浓硫酸 b.品红溶液 c.酸性高锰酸钾溶液d.饱和碳酸氢钠溶液 e.氢氧化钠溶液 f.无水硫酸铜 g.碱石灰 h.五氧化二磷 i.无水氯化钙
请将下列容器中应盛放的试剂序号填入相应空格:
B中_____________,D中______________,E中_____________。
实验过程中,当仪器A内的固体反应完全后,需打开活塞K,向A中通入大量的空气。这样做的目的是______________。所通空气应先经过___________试剂(填上述所供试剂的序号)处理,否则可能引起Na2SO3含量的测量结果比实际值_________(填“偏高”、“偏低”或“没影响”)。
(5)若仪器E在试验完成时增重4.4g,则Na2CO3与Na2SO3的物质的量之比为____。