随着人们生活质量的不断提高,对废电池必须进行集中处理的问题被提到议事日程,其首要原因
| A.利用电池外壳的金属材料 |
| B.防止电池中汞、镉和铅等重金属离子对土地和水源的污染 |
| C.不使电池中渗漏的电解液腐蚀其他物品 |
| D.回收其中的石墨电池 |
用已知物质的量浓度的NaOH溶液测定未知物质的量浓度的盐酸,其操作错误的是
| A.酸式滴定管需用待测盐酸润洗 |
| B.碱式滴定管不用标准碱液润洗 |
| C.滴定过程中不能有液体从锥形瓶溅出 |
| D.滴定结束,读数时要平视读数 |
在固定体积的容器内进行反应2HI(g) 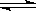 H2(g) + I2(g),达到 平衡状态的标志是
H2(g) + I2(g),达到 平衡状态的标志是
| A.I2(g)的消耗速率等于H2的消耗速率 |
| B.容器中各组分的浓度不随时间变化 |
| C.容器内气体的压强不再变化 |
| D.单位时间内生成n mol H2,同时生成n mol HI |
已知某温度下,几种酸的电离常数如下:Ka(HCN)= 6.2×10-10 mol·L-1、Ka(HF)= 6.8×10-4 mol·L-1、Ka(CH3COOH)= 1.8×10-5 mol·L-1、、Ka(HNO2)= 6.4×10-6mol·L-1。则物质的量浓度都为0.1 mol·L-1的下列溶液中,pH最小的是
| A.NaCN | B.NaF | C.CH3COONa | D.NaNO2 |
下列反应中,属于水解反应且使溶液显酸性的是
A.CH3COOH+OH- CH3COO-+H2O CH3COO-+H2O |
B.HCO3—+ H2O  CO32- + H3O+ CO32- + H3O+ |
C.S2- + H2O HS-+ OH- HS-+ OH- |
D.NH4+ + H2O  NH3·H2O + H+ NH3·H2O + H+ |
下列各组离子一定能在指定环境中大量共存的是
A.在c(H+)=10-10 mol/L的溶液中 Al3+、NH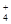 、Cl- 、NO 、Cl- 、NO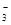 |
B.pH值为1的溶液 Fe2+、Na+ 、SO42-、NO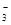 |
| C.水电离出来的c(H+)=10-12mol/L的溶液 K+、HCO3-、Cl-、ClO- |
D.pH值为13的溶液 K+、CO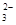 、Na+、[Al(OH)]4- 、Na+、[Al(OH)]4- |