实验室需要1.0mol/L的NaOH溶液,有如下操作步骤:
①把称量好的4.0gNaOH固体放入小烧杯中,加适量蒸馏水溶解。
②把①所得溶液冷却后小心转入一定容积的容量瓶中。
③继续向容量瓶中加蒸馏水至液面距刻度线1 cm~2 cm处,改用胶头滴管小心滴加蒸馏水至溶液凹液面与刻度线相切。
④用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心转入容量瓶,并轻轻摇匀。
⑤将容量瓶瓶塞塞紧,充分摇匀。
请填写下列空白:
(1)操作步骤的正确顺序为(填序号) 。
(2)步骤②所用容量瓶的规格 (填序号)
A.100 mL B.250mL C.500 mL D.1000mL
(3)本实验用到的玻璃仪器除容量瓶、玻璃棒外还有______________________________。
(4)需要使用玻璃棒的操作有________(填序号),其作用为 。
(5)下列操作会使配得的溶液浓度偏低的是 (填序号)
A.容量瓶中原有少量蒸馏水
B.溶液从烧杯转移到容量瓶中后没有洗涤烧杯
C.定容时观察液面俯视
D.配制溶液时,加水超过容量瓶刻度,用胶头滴管将多余溶液吸出
(12分)依据事实,写出下列反应的热化学方程式。
⑴在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为___________________________________________
⑵若适量的N2和O2完全反应,每生成23克NO2需要吸收16.95kJ热量。____________________________________________________________________
⑶用NA表示阿伏加德罗常数,在C2H2(气态)完全燃烧生成CO2和液态水的反应中,每有5NA个电子转移时,放出650kJ的热量。___________________________________
⑷已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为________________________________
已知乳酸的结构简式为 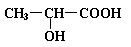 。试回答:
。试回答:
(1)乳酸分子中含有________和_________两种官能团(写名称);
(2)乳酸与金属钠溶液反应的化学方程式为
___________________________________________________________________;
(3)乳酸与Na2CO3溶液反应的化学方程式为
___________________________________________________________________;
(4)当乳酸和浓硫酸共热时,能产生多种酯类化合物,任意写出一种该类产物的结构简式
古代的“药金”外观与金相似,常误以为是金子。冶炼方法如下:将碳酸锌、赤铜(Cu2O)、木炭混合加热至800℃得金光闪闪的“药金”。
(1)“药金”的主要成分是 。
(2)有关冶炼的化学方程式是 、
、
。
海水中含有氯化镁,是镁的重要来源之一。从海水中制取镁,某同学设计了如下步骤:
①把贝壳制成石灰乳
②直接往海水中加石灰乳,沉降、过滤、洗涤沉淀物
③将沉淀物与盐酸反应,结晶、过滤、干燥产物
④将得到的产物熔融后电解。
(1)下列说法不正确的是__________________(填代号)
| A.此法的优点之一是原料来源丰富 |
| B.进行①②③步骤的目的是从海水中提取氯化镁 |
| C.第④步电解制镁是由于镁是很活泼的金属 |
| D.以上制取镁的过程中涉及的反应有分解反应、化合反应和置换反应 |
(2)步骤②不够合理,理由是
实验室利用右图装置进行中和热的测定,请回答下列问题: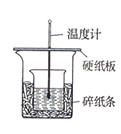
(1)在操作正确的前提下,提高中和热测定准确性的关键是
(2)做1次完整的中和热测定实验,温度计需使用次,
某同学为了省去清洗温度计的麻烦,建议实验时使用两支温度计分别
测量酸和碱的温度,你是否同意该同学的观点,为什么?
(3)请为本实验设计数据记录表格: