氯碱工业是最基本的化学工业之一,离子膜电解法为目前普遍使用的生产方法,其生产流程如下图所示: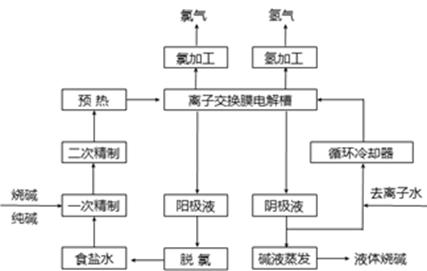
(1)该流程中可以循环的物质是 。
(2)电解法制碱的主要原料是饱和食盐水,由于粗盐水中含有Ca2+、Mg2+、SO42-等无机杂质,所以在进入电解槽前需要进行两次精制,写出一次精制中发生的离子方程式: ,若食盐水不经过二次精制就直接进入离子膜电解槽会产生什么后果: 。
(3)下图是工业上电解饱和食盐水的离子交换膜电解槽示意图(阳极用金属钛网制成,阴极由碳钢网制成)。则B处产生的气体是 ,E电极的名称是 。电解总反应的离子方程式为 。
(4)从阳极槽出来的淡盐水中,往往含有少量的溶解氯,需要加入8%~9%的亚硫酸钠溶液将其彻底除去,该反应的化学方程式为 。
(5)已知在电解槽中,每小时通过1安培的直流电可以产生1.492g的烧碱,某工厂用300个电解槽串联生产8小时,制得32%的烧碱溶液(密度为1.342吨/m3)113m3,电解槽的电流强度1.45 ×104A,该电解槽的电解效率为 。
实验室配制少量银氨溶液的方法是先向洁净的试管中加入溶液,然后逐滴加入生成白色沉淀,反应的离子方程式是①______________________________ ;继续滴加至沉淀恰好溶解,即得银氨溶液,反应的离子方程式为②_________________________________;
( 共3分)把2g甲醛气体溶于6g冰醋酸中,再加入4g葡萄糖得混合物甲;另取5g甲酸甲酯和8g乳酸[CH3CH(OH)COOH]混合,得混合物乙;然后将甲和乙两种溶液按7∶4的质量比混合得丙。则甲中碳元素的质量分数为,乙中氢元素的质量分数为,取60g丙完全燃烧,消耗O2的物质的量为 mol。
(7分)在下列物质中选择相应的序号填空:
①甲烷 ②乙烯 ③乙炔 ④甲苯 ⑤1-丁醇 ⑥乙酸乙酯 ⑦甘氨酸
Ⅰ.分子结构为正四面体的是;
Ⅱ.分子中中心原子采取sp杂化的是;
Ⅲ.能发生水解反应的是;
Ⅳ.能与溴水反应并使其褪色的是;
Ⅴ.分子与分子之间存在氢键的是;
Ⅵ.能发生消去反应的是
Ⅶ.与酸或碱都能反应生成盐的是。
(8分)下图装置中,A是由导热材料制成的密闭容器,B是耐化学腐蚀且易于传热的透明气球,关闭K2,将等量1mol的NO2通过K1、K3分别充A、B中,反应起始时,A、B的体积相同均为a L。已知:2NO2(g) 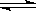 N2O4(g)
N2O4(g) 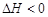
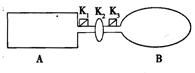
(1)B中可通过判断可逆反应2NO2(g) 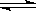 N2O4(g)已经达到平衡。
N2O4(g)已经达到平衡。
(2)若平衡后向A中再充入0.5 mol N2O4,则重新到达平衡后,平衡混合气中NO2的体积分数(填“变小”、“变大”或“不变”)。
(3)若A中到达平衡所需时间为t s,达到平衡后容器内压强为起始压强的0.8倍,则平均反应速率v(NO2)=。
(4)若打开K2,平衡后B的体积缩至0.4a L,则打开K2前,B的体积为。
(10分) 科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池。已知H2(g)、CO(g)和CH3OH(l )的燃烧热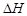 分别为-285.8 kJ·mol-1 、-283.0 kJ·mol-1和-726.5 kJ·mol-1。请回答下列问题:
分别为-285.8 kJ·mol-1 、-283.0 kJ·mol-1和-726.5 kJ·mol-1。请回答下列问题:
(1)用太阳能分解10 mol水消耗的能量是kJ;
(2)甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为;
(3)在容积为2 L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变的
情况下,考察温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300℃) 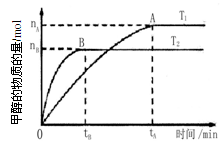
下列说法正确的是(填序号)
①温度为T1时,从反应开始到平衡,生成甲醇的平均速率为n(CH3OH)=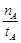 mol·L-1·min-1
mol·L-1·min-1
②该反应在T1时的平衡常数比T2时的小
③该反应为放热反应
④处于A点的反应体系从T1变到T2,达到平衡时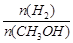 增大
增大
(4)在T1温度时,将1 mol CO2和3 mol H2充入一密闭恒容容器中,充分反应达到平衡后,若CO2的转化率为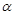 ,则容器内的压强与起始压强之比为.
,则容器内的压强与起始压强之比为.