设NA为阿伏伽德罗常数的数值。下列说法正确的是
| A.0.1 mol·L-1的NaF溶液中所含F-的数目小于0.1NA |
| B.标准状况下,2.24L乙醇中含有的C—H键数目为0.5NA |
| C.0.1 molNa完全被氧化生成Na2O2,转移电子的数目为0.1NA |
| D.0.1 molO3和O2的混合气体中含氧原子数目为0.2NA |
在恒温恒容容器中进行反应A(g)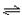 2B(g)
2B(g) +C(g),若A的浓度由0.1 mol·L-1降到0.06 mol·L-1需20 s,那么由0.06 mol·L-1降到0.024 mol·L-1,需要的时间
+C(g),若A的浓度由0.1 mol·L-1降到0.06 mol·L-1需20 s,那么由0.06 mol·L-1降到0.024 mol·L-1,需要的时间
| A.等于18 s | B.等于12  s s |
C.大于18 s | D.小于18 s |
表明金属甲比金属乙活动性强的叙述正确的是
| A.在氧化还原反应中,甲失电子数比乙多 | B.将甲、乙组成原电池时,甲为正极 |
| C.甲不能与盐酸反应放出H2,而乙能 | D.甲、乙最高价氧化物的水化物碱性:甲>乙 |
把下列四种X溶液分别加入四个盛有10 mL 2 mol/L盐酸的烧杯中,均加水稀释到50 mL,此时X和盐酸和缓地进行反应。其中反应速率最大的是
| A.20 mL 3 mol/L 的X溶液 | B.20 mL 2 mol/L 的X溶液 |
| C.10 mL 4 mol/L 的X溶液 | D.10 mL 2 mol/L 的X溶液 |
下列化学反应中,属于放热反应的是
| A. Ba(OH)2·8H2O+NH4Cl(固体) | B.稀盐酸+ Zn |
| C.KClO3受热分解 | D.浓硫酸+H20 |
a、b、c、d、e是同周期的五种元素,a和b的最高价氧化物的水化物显碱性,且碱性b>a, c和d的气态氢化物的还原性d>c,五种元素的原子,得失电子后所形成的简单离子中,e的离子半径最小,则它们的原子序数由小到大的顺序是
| A.b、a、e、d、c | B.e、d、a、b、c | C.a、b、d、c、e | D.c、d、e、a、b |