[化学—选修3:物质结构与性质](15分)
已知A、B、C、D、E五种元素的原子序数依次增大,其中A原子所处的周期数、族序数都与其原子序数相等;B原子核外电子有6种不同的运动状态,s轨道电子数是p轨道电子数的两倍;D原子L电子层上有2对成对电子;E+原子核外有3层电子且各层均处于全满状态。
请填写下列空白。
(1)E元素基态原子的核外电子排布式为_________________。
(2)B、C、D三种元素的第一电离能数值由小到大的顺序为________(填元素符号),其原因为______。
(3)B2A4是重要的基本石油化工原料。B2A4分子中B原子轨道的杂化类型为__________;1 mol B2A4分子中含__________molσ键。
(4)已知D、E能形成晶胞如图所示的两种化合物,化合物的化学式,甲为__________,乙为_____________;高温时,甲易转化为乙的原因为__________________。
实验室用固体烧碱配制500mL 0.32mol·L-1的NaOH溶液。
①需称量______ ____ g的烧碱固体,固体应放在____________中置于天平左盘称量。
②配制过程中,不需要使用的仪器是(填符号)_____________。
A烧杯 B、量筒 C、玻璃棒 D、1000mL容量瓶 E、漏斗
③根据实验的实际需要和②中列出的仪器判断,完成实验还缺少的仪器是_________ (填仪器名称)。
④由于操作上的不规范,下列使所配溶液的物质的量浓度偏低的是_________:偏高的是______:
A称量时药品和砝码位置颠倒
B称量时间过长
C、溶液未冷却即转入容量瓶
D、容量瓶洗净后未烘干
E、定容时俯视刻度线
F、定容后倒转摇匀,发现液面低于刻度线而未加水补充
火力发电厂释放出大量的氮氧化物(NOx)、二氧化硫和二氧化碳等气体会造成环境污染。对燃煤废气进行脱硝、脱硫和脱碳等处理,可实现绿色环保、节能减排、废物利用等目的。
(1)脱硝。利用甲烷催化还原NOx:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1=-574 kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2=-1160 kJ·mol-1
甲烷直接将NO2还原为N2的热化学方程式为。
(2)脱碳。将CO2转化为甲醇的热化学方程式为:
CO2(g)+3H2(g)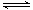 CH3OH(g)+H2O(g)△H3
CH3OH(g)+H2O(g)△H3
①取五份等体积的CO2和H2的混合气体(物质的量之比均为1∶3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH) 与反应温度T的关系曲线如图所示,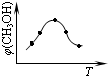
则上述CO2转化为甲醇的反应的△H3__________0(填“>”、“<”或“=”)。
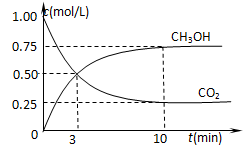
②在一恒温恒容密闭容器中充入1 mol CO2和3 mol H2,进行上述反应。测得CO2和CH3OH(g)的浓度随时间变化如图所示。试回答:0~10 min内,氢气的平均反应速率为mol/(L·min);该温度下,反应的平衡常数的值为;第10 min后,向该容器中再充入1 mol CO2和3 mol H2,则再次达到平衡时CH3OH(g)的体积分数(填变大、减少、不变)。
(3)脱硫。某种脱硫工艺中将废气经处理后,与一定量的氨气、空气反应,生成硫酸铵和硝酸铵的混合物作为副产品化肥。硫酸铵和硝酸铵的水溶液的pH<7,其原因用离子方程式表示为;在一定物质的量浓度的硝酸铵溶液中滴加适量的NaOH溶液,使溶液的pH=7,则溶液中c(Na+) + c(H+)__________c(NO3-) + c(OH-)(填写 “>”“=”或“<”)
A、B、C、D四种元素分布在三个不同的短周期,它们的原子序数依次增大,其中B与C为同一周期,A与D为同一主族,C元素的原子核外电子总数是电子层数的4倍,D是所在周期原子半径最大的元素。又知四种元素分别形成的常见单质在常温常压下有三种是气体,一种是固体。请回答下列问题:
(1)D在元素周期表中的位置是______。
(2) 由A、C两元素可以组成X、Y两种化合物,X在一定条件下可以分解成Y,X的电子式为____。
(3) D与C形成的化合物可与Y反应生成单质Z,该反应的化学方程式为;若有1 mol电子转移,生成Z的物质的量为mol。
(4) 写出实验室制备BA3的化学方程式______________________。将BA3通入溴水中可发生反应,生成一种单质和一种盐,写出该反应的离子方程式。
(5) 已知B2A4可燃烧生成B的单质和Y,以B2A4、O2、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。该电池负极反应是_______________。以石墨为电极,用该电池电解100 mL饱和食盐水,一段时间后,在两极共收集到224 mL气体(标准状况下),此时溶液的pH是(忽略溶液体积的变化)________。
【化学-有机化学基础】A与B在一定条件下反应生成C,进一步反应生成抗氧化剂“安维那”D,其分子式为C10H10O4。A对氢气的相对密度为52,1 mol A与足量NaHCO3反应生成2 mol气体。B属于芳香类化合物。已知:
RCHO+CH2(COOH)2 RCH=C(COOH)2+H2O,
RCH=C(COOH)2+H2O,
RCH=C(COOH)2 RCH=CHCOOH+CO2
RCH=CHCOOH+CO2
(1)C可能发生的反应是____________(填序号)。
| A.氧化反应 | B.水解反应 | C.消去反应 | D.酯化反应 |
(2)等物质的量的C分别与足量的Na、NaHCO3、NaOH反应时消耗Na、NaHCO3、NaOH的物质的量之比是_____________。
(3)A的分子式是____________。
(4)反应①的化学方程式是______________________________________________________。
(5)符合下列条件的D的同分异构体有_______种,写出其中任意一种的结构简式______________。
①在苯环上只有两个取代基;
②在苯环上的一氯取代物只有两种;
③1 mol该同分异构体与足量NaHCO3反应生成2 mol CO2。
(化学---选修物质结构与性质)Q、R、X、Y、Z五种元素的原子序数依次递增。已知:
①Z的原子序数为29,其余的均为短周期主族元素;
②Y原子价电子(外围电子)排布msnmpn
③R原子核外L层电子数为奇数;
④Q、X原子p轨道的电子数分别为2和4。
请回答下列问题:
(1)Z2+ 的核外电子排布式是。
(2)在[Z(NH3)4]2+离子中,Z2+的空间轨道受NH3分子提供的形成配位键。
(3)Q与Y形成的最简单气态氢化物分别为甲、乙,下列判断正确的是。
| A.稳定性:甲>乙,沸点:甲>乙 | B.稳定性:甲>乙,沸点:甲<乙 |
| C.稳定性:甲<乙,沸点:甲<乙 | D.稳定性:甲<乙,沸点:甲>乙 |
(4)Q、R、Y三种元素的第一电离能数值由小到大的顺序为.(用元素符号作答)
(5)Q的一种氢化物相对分子质量为26,其中分子中的σ键与π键的键数之比为。
(6)五种元素中,电负性最大与最小的两种非金属元素形成的晶体属于。