(8分)短周期元素X、Y、Z、W在周期表中的位置关系如图所示。已知在同周期元素的常见简单离子中,W的离子半径最小,X、Y、Z、W的单质及其化合物在日常生活中用途极其广泛。
(1)X元素在元素周期表中的位置是___________________。
(2)X、Y、Z元素的氢化物均有两种或两种以上。
①液态YH3的电离方式与液态H2Z类似,则液态YH3中阴离子的电子式为____________________;
②在一定条件下X2H4与H2Z可发生反应,化学方程式为_____________,反应类型为__________。
(3)以W为材料制成的容器在空气中具有自我保护作用,这种容器不能贮存强碱溶液,用离子方程式表示其原因为____________________________________________。
(4)超细WY粉末被应用于大规模集成电路领域。其制作原理为W2Z3、Y2、X在高温下反应生成两种化合物,这两种化合物均由两种元素组成,且原子个数比均为1:l;其反应的化学方程式为___。
根据图示填空。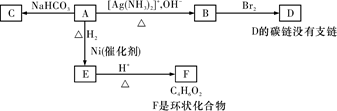
(1)化合物A含有的官能团是 。
(2)1mol A与2mol H2反应生成1mol E,其反应方程式是 。
(3)与A具有相同官能团的A的同分异构体的结构简式是
。
(4)B在酸性条件下与Br2反应得到D,D的结构简式是
。
(5)F的结构简式是 。由E生成F的反应类型是 。
(6)写出A―→B的化学方程式 。
某同学用图示装置进行铁和稀硝酸反应的实验并进行相关的实验探究。
a.向广口瓶内注入足量热NaOH溶液,将盛有a g纯铁粉的小烧杯放入瓶中。
b.关闭止水夹,点燃红磷,伸入瓶中,塞好胶塞。
c.待红磷充分燃烧,一段时间后打开分液漏斗旋塞,向烧杯中滴入300mL 6mol/L的稀硝酸,铁粉恰好完全溶解。
(一)气体产物成分探究:
(1)燃烧红磷的目的是 。
(2)为证明气体产物为NO,步骤c后还缺少的一步主要操作是 。
(二)产物中铁元素价态探究:
(1)提出合理假设:
假设1:产物只有+3价铁;
假设2: ;
假设3: 。
(2)设计实验:分别取小烧杯中反应后溶液装入两支试管甲、乙,在甲试管中滴加酸性高锰酸钾溶液;在乙试管中滴加KSCN溶液,观察现象。推测实验现象与结论:
①若现象为: ,则假设1正确;
②若现象为: , 则假设2正确;
则假设2正确;
③若现象为: ,则假设3正确。
(3)a值范围为 。
X、Y、Z、L、M五种元素的原子序数依次增大。X、Y、Z、L是组成蛋白质的基础元素,M是地壳中含量最高的金属元素。回答下列问题:
(1)五种元素的原子半径从大到小的顺序是 (用元素符号表示)。
(2)X与Z形成的3∶1的化合物A,它与Z的最高价氧化物对应的水化物B反应的化学方程式 ,该水溶液显 性,用离子方程式解释原因 。
(3)硒是人体必需的微量元素,与L同一主族,其最高价氧化物对应的水化物化学式为 。该元素固体单质与H2反应生成0.5 mol气态氢化物时吸收了14.87kJ的热量,请写出1mol该物质与氢气化合的热化学方程式 。
(4)用M单质作阳极,石墨作阴极,NaHCO3溶液作电解液进行电解,生成难溶物R,R受热分解生成化合物Q 。写出阳极生成R的电极反应式:  ;由R生成Q的化学方程式: 。
;由R生成Q的化学方程式: 。
请用单线桥表示该氧化还原反应,并指出该反应的还原产物。
2Na2O2 +2CO2 ===2Na2CO3+O2,还原产物是 。
已知A-K是中学化学中常见有机物,其中G不能使酸性高锰酸钾溶液褪色,它们之间有如下关系。
试回答下列问题:
(1)写出实验室制取A的化学方程式:_________________________________________;
(2)写出D→E的化学方程式:________________________________________________;
(3)B在一定条件下可通过加聚合成一种重要的塑料,写出该合成反应的方程式:
_____________________________________ _________________________________;
_________________________________;
(4)(2分)写出化合物F的结构简式:酯K的结构简式:__________________;
(5)请写出F+J→K的化学反应方程式