下列各组离子在指定条件下,一定能大量共存的是
| A.使石蕊试液变红色的溶液中:K+、Na+、CO32-、NO3- |
| B.在酸性高锰酸钾溶液中:Na+、NH4+、I-、Br- |
| C.c(H+)=10-1 mol/L的溶液中:Cu2+、Al3+、SO42-、NO3- |
| D.水电离出的c(H+)=10-12 mol/L的溶液中:Na+、Mg2+、Cl-、SO42- |
下列叙述正确的是()
| A.可燃冰晶体中(8CH4·46H2O)CH4与H2O 分子之间以及H2O 与H2O 间都以氢键结合 |
| B.氨气易液化,是因为氨分子之间存在氢键 |
| C.含有阳离子的晶体一定是离子晶体 |
| D.金属晶体的熔沸点一定比分子晶体高 |
下表为元素周期表前四周期的一部分,下列关于R、W、X、Y、Z五种元素的叙述中正确的是()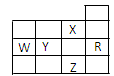
| A.W元素的第一电离能小于Y元素的第一电离能 |
| B.Y、Z的阴离子电子层结构都与R原子的相同 |
| C.最高价含氧酸的酸性,Y对应的酸性强于W |
| D.P亚层未成对电子最多的是Z元素 |
下列关于杂化轨道的叙述中,不正确的是()
| A.分子中中心原子通过SP3杂化轨道成键时,该分子不一定为正四面体结构 |
| B.杂化轨道只用于形成σ键或用于容纳未参与成键的孤电子 |
| C.H2SO4硫酸分子中三种原子均以杂化轨道成键 |
| D.N2分子中N原子没有杂化,分子中有一个σ键、2个π键 |
下列物质性质的变化规律与分子间作用力有关的是()
| A.HF、HCl、HBr、HI的热稳定性依次减弱 |
| B.金刚石的硬度大于硅,其熔、沸点也高于硅 |
| C.NaF、NaCl、NaBr、Nal的熔点依次降低 |
| D.F2、Cl2、Br2、I2的熔、沸点逐渐升高 |
下列说法正确的是()
| A.任何一个能层最多只有s、p、d、f四个能级 |
| B.用n表示能层序数,则每一能层最多容纳电子数为2n2 |
| C.核外电子的运动的概率分布图(电子云)就是原子轨道 |
| D.电子的运动状态可从能层、能级、轨道3个方面进行描述 |