X、Y、Z、W均为短周期元素,它们在元素周期表中相对位置如图所示,若Z原子的最外层电子数是第一层电子数的3倍,下列说法正确的是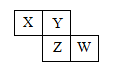
| A.Y单质与氢气反应较Z剧烈 | B.最高价氧化物对应水化物酸性W比Z强 |
| C.X单质氧化性强于Y单质 | D.X与W的原子核外电子数相差9 |
将Fe、FeO、Fe3O4混合物均分成两等份,在相同条件下,一份用足量H2还原,参加反应H2的体积为V1,另一份用足量稀HNO3处理得NO气体体积为V2,若V1:V2=3:1,则原混合物中各成分的物质的量之比可能为
| A.2:3:2 | B.3:2:2 | C.1:2:3 | D.3:2:1 |
据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如右图所示。下列说法正确的是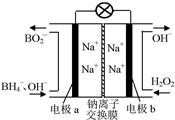
| A.电池放电时Na+从b极区移向a极区 |
| B.每消耗3 mol H2O2,转移的电子为3 mol |
| C.电极a采用MnO2,MnO2既作电极材料又有催化作用 |
| D.该电池的负极反应为:BH4-+8OH--8e-=BO2-+6H2O |
甲、乙、丙、丁四种易溶于水的物质分别有NH4+、Ba2+、Mg2+、H+、OH-、Cl-、HCO3-、SO42-中的不同阳离子和阴离子各一种组成。已知:①将甲溶液分别与其他三种物质的溶液混合,均有白色沉淀生成;②0.1mol/L乙溶液中c(H+)>0.1mol/L;③向丙溶液中滴入AgNO3溶液有不溶于稀HNO3的白色沉淀生成,下列结论不正确的是
| A.甲溶液含有Ba2+ | B.乙溶液含有SO42- |
| C.丙溶液含有Cl- | D.丁溶液含有Mg2+ |
常温时,下列溶液的pH或微粒的物质的量浓度关系正确的是
A.某溶液中由水电离出的c(H+)=1×10-amol/L,若a>7时,该溶液pH一定为14-a
B.等体积、等物质的量浓度的Na2CO3溶液与NaHCO3溶液混合:
3c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3)
C.将0.2 mol/L的某一元酸HA溶液和0.1 mol/L NaOH溶液等体积混合后溶液pH大于7,则反应后的混合液: c(HA)>C(Na+)>c(A-)
D.pH=3的二元弱酸H2R溶液与pH=11的NaOH溶液混合后,混合液的pH等于7,则反应后的混合液:2c(R2-)+c(HR-)>c(Na+)
利用碱性氧化性溶液的氧化作用,在钢铁表面形成一层Fe3O4薄膜,保护内部金属免受腐蚀,这种方法叫做烤蓝。烤蓝时发生如下反应:
①3Fe+NaNO2+5NaOH===3Na2FeO2+H2O+NH3↑
②Na2FeO2+NaNO2+H2O===Na2Fe2O4+NH3↑+NaOH(未配平)
③Na2FeO2+Na2Fe2O4+2H2O===Fe3O4+4NaOH
下列说法中不正确的是
| A.Fe3O4既可看做是氧化物,又可看做是亚铁盐 |
| B.反应②配平后,H2O的化学计量数为3 |
| C.反应③是非氧化还原反应 |
| D.碱性条件下,NaNO2的氧化性比Na2FeO2、Na2Fe2O4都强 |