(14分)某兴趣小组的学生根据Mg与CO2反应原理推测钠也能在CO2中燃烧,为了确定其产物并进行试验论证,某同学设计了下列装置进行试验(已知PdCl2能被CO还原为Pd),请回答下列问题: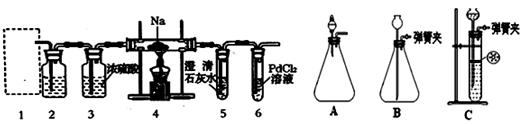
(1)上图装置2中应盛放__________溶液.
(2)为了使反应随开随用,随关随停,上图方框内应选用_____装置(填上图字母代号).
(3)检查装置的气密性完好并装好药品后,在点燃酒精灯前,应先进行1装置的操作,待装置______(填数字编号)中出现_______________现象时,再点燃酒精灯.
(4)①若装置6中有黑色沉淀(Pd)生成,装置4中残留固体(只有一种物质)加盐酸后有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式为_________.
②若装置6中溶液无明显现象,装置4中残留固体(有两种物质)加盐酸后有能澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式为_____________.
下列是用98%的浓H2SO4(ρ=1.84g/cm3)配制500mL 0.5mol∙L-1的稀硫酸的实验操作,请按要求填空:
(1)实验中量取浓硫酸的体积为_________mL。
(2)如果实验室有10mL、20mL、50mL的量筒,应选_______规格的量筒最好,如果量取浓硫酸时仰视读数,所配溶液浓度将(填“偏高”、“偏低”或“无影响”)__________。
(3)将量取的浓硫酸沿烧杯内壁慢慢注入盛有约少量水的烧杯里,并不断搅拌,搅拌的目的是_____________________。
(4)将冷却至室温的上述溶液沿玻璃棒注入_______中,并用50mL蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液要转入到容量瓶中,并振荡;在转移过程中有少量液体洒在桌子是,则最终所配浓度将(填“偏高”、“偏低”或“无影响”)__________。
(5)加水至距刻度线1~2cm处,改用______加水至刻度线,使溶液的凹液面恰好跟容量瓶刻度线相平,把容量瓶塞好,反复颠倒振荡,摇匀溶液。
下图为铜丝与浓硫酸反应并验证其产物性质的实验装置。
(1)①中反应的化学方程式是_________________________。
(2)②中饱和NaHSO3溶液的作用是除去__________。加热一段时间后,③中溶液依然澄清,想要立即终止铜与硫酸的反应,最恰当的方法是___________。
a.上移铜丝,使其脱离硫酸 b.撤去酒精灯 c.拔去橡胶塞倒出硫酸
(3)反应停止后,待装置冷却,把③取下后将其中溶液分成两份做如下实验:
| 加入试剂 |
现象 |
反应的离子方程式 |
|
| 第一份 |
加入NaOH溶液 |
有白色沉淀生成 |
_______________ |
| 第二份 |
加入氯水 |
有白色沉淀生成 |
_______________ |
完成上述反应的离子方程式。
(4)上述实验结束后,发现①中试管内有少量白色固体出现,冷却后将试管中的物质缓缓倒入水中,溶液呈蓝色。取少量蓝色溶液于试管中,滴加NaOH溶液过量,出现的现象是_________________。
亚硝酸钠在漂白、电镀等方面应用广泛。现以木炭、浓硝酸、水和铜为原料生成的一氧化氮与过氧化钠反应制备亚硝酸钠的装置如右图所示(部分夹持装置略)。已知:
①3NaNO2+3HCl=3NaCl+HNO3+2NO↑+H2O
②酸性条件下,NO与NO3-都能与MnO4-反应生成NO3-和Mn2+;
完成下列填空:
(1)写出a仪器的名称___________________________。
(2)为避免B中逸出的气体中混有的杂质气体与Na2O2反应,应在B、C装置间增加一个装置,则该装置中盛放的药品名称为__________________。
(3)写出NO与Na2O2在常温下生成NaNO2的化学反应方程式______________________;当该反应中转移0.1mole-时,理论上吸收标准状况下NO的体积为__________L。
(4)将11.7g过氧化钠完全转化成亚硝酸钠,理论上至少需要木炭__________g。
(5)NO2易溶于水。将体积为V mL的试管充满NO2后倒扣在水中,见右图。
①NO2溶于水的化学方程式是_________________________。
②使试管中NO2完全被水吸收的操作是______________________________。
某小组同学通过对比实验了解Na2CO3和NaHCO3性质的异同,下表是他们撰写的实验报告的一部分。
| 实验序号 |
实验步骤(内容) |
现象 |
| ① |
在贴有标签a、b的试管中分别加入1.0gNa2CO3固体和NaHCO3固体,观察外观。 |
|
| ② |
继续向两试管中分别加入10.0mL水,用力振荡,观察现象。 |
|
| ③ |
再分别向两试管中滴加2滴酚酞溶液,观察现象。 |
溶液变红 |
| ④ |
加热大试管一段时间。(注:棉花球沾有无水硫酸铜粉末) |
|
 |
(1)请帮助该小组同学完成实验报告中放入内容________________________。
(2)已知:20℃时Na2CO3的溶解度为20.5g。由实验_________(填实验序号)现象可知,20℃时NaHCO3的溶解度小于20.5g;如果向饱和Na2CO3溶液中不断通入CO2气体,现象是____________,化学方程式是________________________。
(3)由实验④可以得出结论是____________,用化学方程式说明得出结论的原因__________________。
某学习小组利用下图所示装置制备氨气,并探究氨气的性质(部分仪器略去)。
请回答下列问题:
(1)写出以A装置制备氨气的化学方程式:__________________
(2)用B装置收集氨气时,氨气的进气口是__________(填“a”或“b”)。
(3)B装置中烧瓶已收集满氨气,若要使之形成喷泉,操作方法是__________。若观察到装置B中的烧瓶内产生了红色喷泉,则说明氨气具有的性质是_________。
(4)为防止环境污染,以下装置(盛放的液体均为水)可用于吸收多余氨气的是_________(填序号)。
(5)氨气在催化剂并且加热时会被空气氧化,这是工业制硝酸的第一步反应,写出该反应的化学方程式:_________。