(选做)【化学—选修5:有机化学基础】
没食子酸丙酯简称PG,结构简式为  ,是白色粉末,难溶于水,微溶于棉子油等油脂,是常用的食用油抗氧化剂。
,是白色粉末,难溶于水,微溶于棉子油等油脂,是常用的食用油抗氧化剂。
(1)PG的分子式为 ,请写出PG分子中所含官能团的名称 ,1molPG与足量氢氧化钠溶液完全反应时,消耗的氢氧化钠的物质的量是 。
PG可发生如下转化:
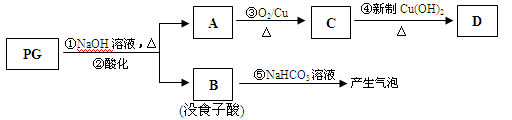
(2)A的结构简式为 ,1mol没食子酸最多可与 mol H2加成。
(3)上图的有关变化中,属于氧化反应的有(填序号) 。
(4)从分子结构或性质上看,PG具有抗氧化作用的主要原因是(填序号) 。
| A.含有苯环 | B.含有羧基 | C.含有酚羟基 | D.微溶于食用油 |
(5)反应④的化学方程式为:
(6)B有多种同分异构体,写出其中符合下列要求的同分异构体的结构简式:
i.含有苯环,且苯环上的一溴代物只有一种;ii.既能发生银镜反应,又能发生水解反应。
在20 L的恒容密闭容器中,加入3 mol SO3(g)和1 mol氧气,在某温度下使其反应,反应至4 min时,氧气的浓度为0.06 mol/L,反应至8 min时达平衡状态。
(1)在0~4 min内生成O2的平均速率v(O2)=___ mol/(L·min)。
(2)整个过程中,各物质的浓度与时间的关系如图所示,则该温度下的平衡常数K=______。
(3)若起始时按下表数据投料,相同温度下达到平衡时,三氧化硫浓度大于0.05 mol/L的是______,此时的平衡常数与(2)中相比________(填“增大”、“减小”或“不变”)。
| 选项 |
A |
B |
C |
D |
| SO3 |
1 mol |
3 mol |
3 mol |
0 mol |
| SO2 |
2 mol |
1.5 mol |
0 mol |
6 mol |
| O2 |
2 mol |
1 mol |
0 mol |
5 mol |
反应aA(g)+bB(g)  cC(g)+dD(g)在容积不变的密闭容器中达到平衡,且起始时A与B的物质的量之比为 a∶b。则
cC(g)+dD(g)在容积不变的密闭容器中达到平衡,且起始时A与B的物质的量之比为 a∶b。则
(1)平衡时A与B的转化率之比是__________。
(2)若同等倍数地增大A、B的物质的量浓度,要使A与B的转化率同时增大,(a+b)与(c+d)所满足的关系是(a+b)______(c+d)(填“>”、“=”、“<”或“没关系”)。
(3)设定a=2 ,b=1,c=3,d=2,在甲、乙、丙、丁4个相同的容器中A的物质的量依次是2 mol、1 mol、2 mol、1 mol,B的物质的量依次是1 mol、1 mol、2 mol、2 mol,C和D的物质的量均为0。则在相同温度下达到平衡时,A的转化率最大的容器是______(填容器序号,下同) 。
t℃时,将3molA和2molB气体通人体积为2L的密闭容器中(容积不变),发生如下反应:3A(气)+B(气)  xC(气),2min时反应达到平衡状态(温度不变),剩余1.8molB,并测得C的浓度为O.4mol/L,请填写下列空白:
xC(气),2min时反应达到平衡状态(温度不变),剩余1.8molB,并测得C的浓度为O.4mol/L,请填写下列空白:
(1)x=__________。
(2)比较达到平衡时,A、B两反应物的转化率:α(A)________α(B)(填>、=或<)
(3)若继续向原平衡混合物的容器中通人少量氦气(氦气和A、B、C)都不反应)后,下列说法中正确的是____________(填写字母序号)
A.化学平衡向正反应方向移动
B.化学平衡向逆反应方向移动
C.化学平衡不会发生移动
D.正、逆反应的化学反应速率将发生同等程度的改变
(4)在t℃时,若向原平衡混合物的容器中再充入amolC,欲使达到新的平衡时,各物质的物质的量分数与原平衡相同,则至少应再充入__________(填A或B)________mol(用a表示),
有pH=1的①盐酸 ②硫酸 ③醋酸
(1)设三种溶液的物质的量浓度分别为a、b、c,则其大小关系为 。
(2)同体积的三种溶液与足量的NaOH溶液反应生成盐的物质的量分别为a、b、c,则其大小关系为 。
(3)完全中和物质的量浓度和体积都相同的NaOH溶液时,需三种酸溶液的体积分别为a、b、c,则其大小关系为 。
pH=12的NaOH溶液100mL,要使它的pH为11。(体积变化忽略不计)
(1)如果加入蒸馏水,应加_________mL;
(2)如果加入pH=10的NaOH溶液,应加_________mL;