下列物质A、B、C、D都是初中化学中的常见物质,它们之间具有如图所示的转化关系(反应条件、有些反应物或产物已略去).其中A与B的组成元素相同,C可使带火星的木条复燃,D是一种无色气体单质.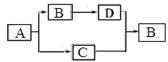
(1)写出下列D的化学式: .
(2)C与D反应的基本类型是______________.
(3)写出C的一种用途___________________.
(4)写出B转化为D的化学方程式 .
小明向氢氧化钠溶液中滴加稀盐酸,发现没有明显现象.为了判断两者是否恰好完全反应,他取少量反应后的溶液加入试管中,滴加几滴无色酚酞试液,振荡后观察到酚酞试液不变色.
(1)根据上述现象,小明得出“两种物质恰好完全反应”的结论.小白认为小明的结论是不合理的,其理由是________.
(2)小白利用pH试纸测反应后溶液的pH,以确定两者是否恰好完全反应.请你选用其他试剂再设计一个实验,以验证氢氧化钠和盐酸是否恰好完全反应(要求写出选用的试剂、可能观察到的现象和相应的结论)________.
(3)小白为了继续探究“在氢氧化钠与盐酸反应的过程中,溶液的pH是如何变化的”这一问题,进行如下实验:在一定量的氢氧化钠溶液中逐渐滴加盐酸,用pH试纸测定溶液的pH,记录数据如下表:
| 盐酸的体体/mL |
0 |
10 |
19.5 |
20 |
20.5 |
30 |
40 |
| pH |
13 |
12 |
10 |
7 |
3 |
2 |
1 |
下图中能合理表示该反应过程中溶液pH变化的是________.
图是甲、乙两种物质的溶解度曲线,请结合该图回答问题:
(1)________℃时,甲、乙两种物质的溶解度相等.
(2)溶解度随温度升高而降低的物质是________(填“甲”或“乙”).
(3)可使甲物质从其饱和溶液中结晶析出的方法是________.
(4)t2℃时,分别将甲、乙两种物质的饱和溶液降温到t1℃,甲溶液的溶质质量分数________(填“大于”“等于”或“小于”)乙溶液的溶质质量分数.
(5)小明同学用甲物质进行以下实验:
①实验过程中,B、C、D对应的溶液为不饱和溶液的是________.
②向B对应的溶液中再加入30g甲固体的过程中,发现固体全部溶解,一段时间后又有部分固体析出.你认为“全部溶解”的原因是________________________________.
下表是KNO3、NaCl在不同温度下的溶解度(单位:g).
| 温度(℃) |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
80 |
90 |
100 |
| KNO3 |
13.3 |
20.9 |
32 |
45.8 |
64 |
85.5 |
110 |
138 |
169 |
202 |
246 |
| NaCl |
35.7 |
35.8 |
36 |
36.3 |
36.6 |
37 |
37.3 |
37.8 |
38.4 |
39 |
39.8 |
(1)以上两物质溶解度的变化受温度影响较小的是________.
(2)30℃时,KNO3的溶解度是________g.
(3)KNO3溶液中含有少量NaCl时,可通过________的方法提纯.
(4)对(3)析出的晶体和剩余溶液描述正确的是________(填写编号).
Ⅰ.剩余溶液一定是KNO3的饱和溶液
Ⅱ.剩余溶液一定是NaCl的不饱和溶液
Ⅲ.上述方法可以将两者完全分离
Ⅳ.析出的晶体中只含有KNO3
(5)在一定温度下,将含69g KNO3、18g NaCl的混合物完全溶解在50g水中.改变温度使KNO3析出,NaCl不析出,则温度T(℃)的范围是________(硝酸钾和氯化钠溶解度互不影响).
图是氯化钠和硝酸钾两种固体物质的溶解度曲线.
某兴趣小组为了研究NaCl和KNO3的溶解和结晶,做了两组实验(室温下),其过程如下:
[第一组]
[第二组]
(1)①中溶质的质量分数为________________,⑨的现象是________________.
(2)第一组实验中操作a为________,所得氯化钠固体质量增多可能是下列原因中的(填字母序号)________.
| A.溶解NaCl固体时,没有用玻璃棒搅拌 |
| B.称量5g NaCl固体后,称量纸上仍留有固体 |
| C.蒸发时,未及时停止加热,有固体溅出 |
| D.蒸发后所得NaCl固体中仍含有水分 |
(3)上述实验过程中一定属于饱和溶液的是(填数字序号,下同)________,溶质与溶剂质量比一定相等的是________.
人类的生产生活离不开金属,下列三种金属使用的先后顺序依次为:铜、铁、铝.
(1)金属被使用的先后顺序跟________(填序号)选项关系最大.
①地壳中金属元素的含量;②金属的导电性;③金属的活动性.
(2)为探究锰与铁的金属活动性,在相同温度下,取大小相同、表面光亮的两种金属薄片,分别投入等体积、等溶质的质量分数的足量稀盐酸中(反应后Mn显+2价),请回答:
| 金属 |
铁 |
锰 |
| 与稀盐酸反应现象 |
放出气泡速率缓慢 |
放出气泡速率较快 |
| 结论 |
活动性铁________锰(填“>”或“<”) |
除了比较与酸反应产生气体速率的快慢,请你再举出一种可比较这两种金属活动性强弱的方法(写出所需药品即可):________________________________________________.
(3)将一定量的铝加入到硫酸亚铁和硫酸铜的混合溶液中,充分反应后过滤,向滤渣中加入盐酸,有气泡产生.则滤渣中一定有的物质是________________.(填化学式)