17.在一定条件下,CO和CH4燃烧的热化学方程式分别为:
2CO(g) + O2(g) = 2CO2(g) △H = —566 kJ/mol
CH4(g) + 2 O2 (g) =" C" O2 (g) + 2H2O(l) △H = —890 kJ/mol
由1molCO和3molCH4组成的混和气在上述条件下完全燃烧时,释放的热量为
| A.2912kJ | B.2953kJ | C.3236kJ | D.3867kJ |
某有机物样品的质荷比如下图所示(假设离子均带一个单位正电荷,信号强度与该离子的多少有关),则该有机物可能是()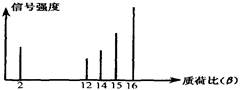
| A.甲醇 | B.甲烷 | C.丙烷 | D.乙烯 |
欲除去下列物质中混入的少量杂质(括号内物质为杂质),不能达到目的的是
| A.乙酸乙酯(乙酸):加饱和碳酸钠溶液,充分振荡静置后,分液 |
| B.乙醇(水):加入新制生石灰,蒸馏 |
| C.苯甲酸(NaCl):加水,重结晶 |
| D.乙酸(乙醇):加入金属钠,蒸馏 |
分子式为C5H12O的饱和一元醇,其分子中有两个-CH3、两个-CH2-、一个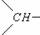 和一个-OH,它的可能结构式有
和一个-OH,它的可能结构式有
| A.2种 | B.3种 | C.4种 | D.5种 |
有机物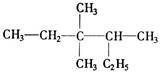 的正确命名为
的正确命名为
| A.2-乙基-3,3-二甲基-4-乙基戊烷 | B.3,3-二甲基-4-乙基戊烷 |
| C.3,3,4-三甲基已烷 | D.2,3,3-三甲基已烷 |
已知丙烷的二氯代物有四种异构体,则其六氯代物的异构体数目为
| A.2种 | B.3种 | C.4种 | D.5种 |