22、(9分)依据事实,写出下列反应的热化学方程式。
(1)在101kPa时,H2在1.00molO2中完全燃烧生成2.00mol液态H2O。 放出571.6kJ的热量,表示H2燃烧的热化学方程式为_____ ___ ____。
(2)在25℃、101kPa下,1g甲醇液体燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为_______________________________________
(3)已知:已知:C(s)+O2(g)=CO2(g) ΔH="-437.3" kJ·mol一1
H2(g)+  O2(g)=H2O(g) ΔH="-285.8" kJ·mol一1
O2(g)=H2O(g) ΔH="-285.8" kJ·mol一1
CO(g)+  O2(g)=CO2(g) ΔH="-283.0" kJ·mol一1
O2(g)=CO2(g) ΔH="-283.0" kJ·mol一1
则煤的气化主要反应(碳和水蒸气反应生成一氧化碳和氢气)的热化学方程式是________________
已知粗铜中含有少量的锌、铁、银、金等金属和少量矿物杂质(与酸不反应)。某化学兴趣小组在实验室条件下用以硫酸铜溶液为电解液,用电解的方法实现了粗铜的提纯,并对阳极泥和电解液中金属进行回收和含量测定。
步骤一:电解精制:请回答以下问题:
电解时,粗铜应与电源的极相连。阴极上的电极反应式为。电解过程中,硫酸铜的浓度会(选填:变大、不变、变小)
步骤二:电解完成后,该小组同学按以下流程对电解液进行处理:
阳极泥的综合利用:稀硝酸处理阳极泥得到硝酸银稀溶液,请你写出该步反应的离子反应方程式:。残渣含有极少量的黄金,如何回收金,他们查阅了有关资料,了解到了一些有关金的知识,以下是他们获取的一些信息:
| 序号 |
反应 |
平衡常数 |
| 1 |
Au + 6HNO3(浓)= Au(NO3)3 + 3NO2↑+ 3H2O |
<< 1 |
| 2 |
Au3+ + 4Cl— = AuCl4— |
>>1 |
从中可知,金很难与硝酸反应,但却可溶于王水(浓硝酸与盐酸按体积比1∶3的混合物),请你简要解释金能够溶于王水的原因
(2)滤液含量的测定: 以下是该小组探究滤液的一个实验流程:
则100mL滤液中Cu2+的浓度为mol·L—1,Fe2+的浓度为mol·L—1
A、B、C、D、E都是元素周期表中前20号元素,原子序数依次增大,A是地壳中含量最高的元素,B、C、D同周期,E和其他元素既不在同周期也不在同主族,D的氢化物和最高价氧化物的水化物均为强酸,且B、C、D的最高价氧化物的水化物两两混合均能发生反应生成盐和水。据此回答下列问题:
(1)A和D的氢化物中,沸点较高的是 __________(写出化学式)。
(2)写出A单质的结构式___________。B的最高价氧化物的水化物的电子式__________。
(3)写出E离子的离子结构示意图___________________。元素D在元素周期表中的位置是____________________。
(4)A、D、E可以形成多种盐,其中一种盐中A、D、E三种元素的原子个数比为2:2:1,该盐的名称为 __________。它的水溶液与D的氢化物的水溶液反应可生成D的单质,该离子方程式为______________________。
(1)(6分)已知实验室制备氯气的反应:MnO2 +4HCl(浓)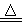 MnCl2 + Cl2↑+ 2H2O其中氧化剂是,还原剂是,氧化产物是,还原产物是,氧化剂和还原剂之比是。
MnCl2 + Cl2↑+ 2H2O其中氧化剂是,还原剂是,氧化产物是,还原产物是,氧化剂和还原剂之比是。
(2)配平氧化还原反应方程式:
__ C2O42-+__MnO4-+__H+=__CO2+__Mn2++__H2O
(3)某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)2、H2O、H2O2已知该反应中H2O2只发生如下过程:H2O2→ O2
①该反应中的氧化剂是。
②该反应中,发生还原反应的过程是→。
③写出该反应的化学方程式,并标出电子转移的方向和数目。
④如反应转移了0.6mol电子,则产生的气体在标准状况下体积为。
(6分)现有以下物质①KNO3溶液②干冰(固态的二氧化碳)③冰醋酸(纯净的醋酸)④铜⑤AgCl固体⑥蔗糖⑦酒精⑧熔融的NaCl⑨氨水⑩盐酸,其中能够导电的是_________________(填序号,下同);属于电解质的是__________________;属于非电解质的是___________________________。
回答下列问题:
(1)下列仪器中:①试管②烧杯③烧瓶④坩埚⑤蒸发皿⑥锥形瓶⑦燃烧匙。可用于直接加热的仪器是________________,需要垫石棉网加热的仪器是____________。(用序号填写)
(2)实验室中需要配制490 mL 0.10 mol·L-1的NaOH溶液。根据题意填空:
A.配制该溶液应选用玻璃仪器有:_________。
B.用托盘天平称取 ________ g NaOH固体。
(3)下列操作导致配制的溶液浓度偏低的是。
A.定容时俯视刻度线
B.将烧杯中溶解后的溶液立刻注入容量瓶,然后再添加蒸馏水至刻度线
C.摇匀定容后,用胶头滴管向容量瓶中滴加蒸馏水至刻度线
D.配制溶液前用蒸馏水润洗容量瓶
E.定容时超出刻度线,用胶头滴管将溶液吸出到刻度线。
F.移液过程中不小心将溶液溅出