氮氧化铝(AlON)是一种高硬度防弹材料,可以在高温下由反应Al2O3+C+N2=2AlON+CO合成,下列有关说法正确的是
| A.氮氧化铝中氮的化合价是-3 |
| B.反应中每生成5.7g AlON 同时生成1.12 L CO |
| C.反应中氧化产物和还原产物的物质的量之比是2:1 |
| D.反应中氮气作氧化剂 |
“绿色化学实验”已走进课堂,下列做法符合“绿色化学”的是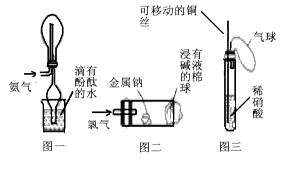
①实验室收集氨气采用图1所示装置
②实验室中做氯气与钠反应实验时采用图2所示装置
③实验室中用玻璃棒分别蘸取浓盐酸和浓氨水做氨气与酸生成铵盐的实验
④实验室中采用图3所示装置进行铜与稀硝酸的反应
| A.②③④ | B.①②③ | C.①②④ | D.①③④ |
一定温度下,难溶强电解质的饱和溶液中存在着沉淀溶解平衡,其平衡常数为
| 物质 |
Fe(OH)2 |
Cu(OH)2 |
Fe(OH)3 |
| Ksp(25℃) |
8.0×10﹣16 |
2.2×10﹣20 |
4.0×10﹣38 |
对于含Fe2(SO4)3、FeSO4和CuSO4各0.5mol的混合溶液1L,根据上表数据判断,说法错误的是
A.向混合溶液中逐滴加入NaOH溶液,最先看到红褐色沉淀
B.向溶液中加入双氧水,并用CuO粉末调节pH,过滤后可获较纯净的CuSO4溶液
C.该溶液中c(SO42﹣):[c(Fe3+)+c(Fe2+)+c(Cu2+)]=5:4
D.将少量FeCl3粉末加入含Cu(OH) 2的悬浊液中,其中c(Cu2+)增大
X、Y、Z、W四种短周期元素在元素周期表中的相对位置如图所示,这四种元素原子的最外层电子数之和为20,下列判断正确的是
| W |
X |
Y |
| Z |
A.四种元素的原子半径:rZ>rX>rY>rW
B.四种元素形成的单质最多有6种
C.四种元素均可与氢元素形成电子总数为18的分子
D.四种元素中,Z的最高价氧化物对应的水化物酸性最强
如图所示是298 K时,N2与H2反应过程中能量变化的曲线图 ,下列叙述错误的是
| A.加入催化剂,不能改变该化学反应的反应热 |
| B.b曲线是加入催化剂时的能量变化曲线 |
C.该反应的热化学方程式为:N2(g)+3H2(g) 2NH3(g),ΔH=-92 kJ/mol 2NH3(g),ΔH=-92 kJ/mol |
| D.在温度、体积一定的条件下,通入1 mol N2和3 molH2反应后放出的热量为92kJ |
下列化合物中与自身类别相同的同分异构体数目(不考虑立体异构)最多的是
| A.戊烷 | B.戊醇 | C.戊烯 | D.乙酸丙酯 |