(每空2分,共14分)已知苯甲醛在一定条件下可以通过Perkin反应生成肉桂酸(产率45%~50%),另一个产物A也呈酸性,反应方程式如下: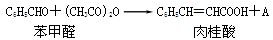
(1)Perkin反应合成肉桂酸的反应式中,反应物的物质的量之比为1:1,产物A的名称是 。
(2)一定条件下,肉桂酸与乙醇反应生成香料肉桂酸乙酯,其反应方程式为 。
(3)取代苯甲醛也能发生Perkin反应,相应产物的产率如下:
| 取代苯甲醛 |
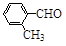 |
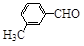 |
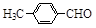 |
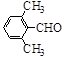 |
| 产率(%) |
15 |
23 |
33 |
0 |
| 取代苯甲醛 |
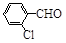 |
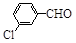 |
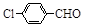 |
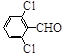 |
| 产率(%) |
71 |
63 |
52 |
82 |
可见,取代基对Perkin反应的影响有(写出3条即可):
①________________________________
②___________________ _
③________________________________
(4)溴苯(C6H5Br)与丙烯酸乙酯(CH2=CHCOOC2H5)在氯化钯(PbCl2)催化下可直接合成肉桂酸乙酯,该反应属于Beck反应,是芳香环上的一种取代反应,其反应方程式为 ____。
(5)Beck反应中的有机产物不能发生的反应是__________(填字母)。
(A)加成反应 (B)取代反应 (C)氧化反应 (D)消去反应
A是一种重要的化工原料,它的产量可以衡量一个国家石油化工水平的高低。A、B、C、D在一定条件下存在如下转化关系(部分反应条件、产物被省略)。
(1)工业上,由石油获得石蜡油的方法是_________,由石蜡油获得A是________变化。
(2)写出A→B的反应方程式:该反应的类型是____________________写出反应B+C→D的化学方程式:____________________________
该反应的类型是。
(3)使1molA与氯气发生完全加成反应,然后使该加成反应的产物与氯气在光照的条件下发生完全取代反应,则两个过程中消耗的氯气的总的物质的量是mol
(4)实验室制备D的实验装置图如图所示:收集产物的试管中盛放的液体为;该溶液的作用有:①除掉产物中的和杂质;②
(5)在制备乙酸乙酯过程中,往往加入的乙酸和乙醇的量要比理论计算量多得多,请解析其中可能存在的原因:
①________________________
②________________________
、(1)有机化合物的结构简式可进一步简化,如: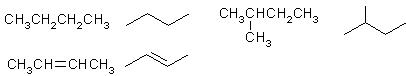
写出下列物质的分子式:
①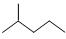 分子式用系统命名法对该有机物进行命名_______________
分子式用系统命名法对该有机物进行命名_______________
② 分子式
分子式
③ 分子式______________
分子式______________
(2)除去下列物质中的杂质(括号内为杂质),填入所用试剂和分离方法。
①乙烯(SO2),试剂,分离方法______________
②苯(溴),试剂,分离方法______________
下表是A、B、C、D、E五种有机物的有关信息:
回答下列问题:
(1)A~E中,属于烃的是(填字母)。
(2)A能使溴的四氯化碳溶液褪色,发生反应的化学方程式为。
(3)C催化氧化生成D的化学方程式为。
(4)有机物B具有的性质是 (填序号)。
①无色无味的液体;
②有毒;
③不溶于水;
④密度比水大;
⑤能使酸性KMnO4溶液和溴水褪色
(5)E的水溶液能使紫色石蕊试液变红,说明E的水溶液显酸性,现设计一个实验来比较E与碳酸酸性的强弱,则该实验的原理是 (用化学方程式说明)。
《茉莉花》是一首脍炙人口的江苏民歌。茉莉花香气的成分有多种,乙酸苯甲酯(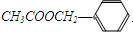 )是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成。一种合成路线如下:
)是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成。一种合成路线如下: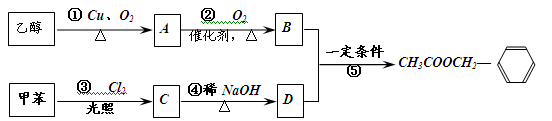
(1)在①②③④⑤五个反应中,属于取代反应的是:(填序号);
(2)B中的含氧官能团的名称是:。
(3)D的含苯环的同分异构体中,能使FeCl3溶液显紫色的有种;
(4)反应⑤ 中120克B与足量的D反应,若B的转化率为60%,则生成乙酸苯甲酯克。
(5)写出乙酸苯甲酯的符合条件的同分异构体的结构简式(写其中一种)。
①含苯环,能发生水解反应和银镜反应;
②苯环上有两种不同化学环境的氢原子
有机物A为无色粘稠液体,易溶于水。为研究A的组成与结构,进行了如下实验:
| 实 验 步 骤 |
解 释 或 实 验 结 论 |
| (1)称取A 9.0g,升温使其汽化,测其密度是相同条件下H2的45倍。 |
试通过计算填空:(1)A的相对分 子质量为:。 |
| (2)将此9. 0gA在足量纯O2充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4g和13.2g。 |
(2)A的分子式为:。 |
| (3)另取A 9.0g,跟足量的NaHCO3粉末反应,生成2.24LCO2(标准状况),若与足量金属钠反应则生成2.24LH2(标准状况)。 |
(3)用结构简式表示A中含有的官能团:。 |
(4)A的核磁共振氢谱如下图: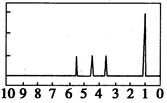 |
(4)A中含有种氢原子。 |
| (5)综上所述,A的结构简式。 |