如图所示,将两烧杯用导线如图相连,Pt、Cu、Zn、C分别为四个电极,当闭合开关后,则以下叙述正确的是
| A.C电极为电解池的阳极 |
| B.Cu电极附近OH-浓度增大 |
| C.Na+移向Pt电极 |
| D.Pt电极上有O2生成 |
在化学反应中,有时存在“一种物质过量,另一种物质仍不能完全反应”的特殊情况。下列反应中属于这种情况的是
①过量的锌与18mol/L硫酸溶液反应
②过量的氢气与少量的N2在催化剂存在下充分反应
③浓盐酸与过量的MnO2
④过量的铜与浓硫酸
⑤过量银与稀硝酸
⑥过量的稀盐酸与块状石灰石
| A.①④⑤ | B.②③⑤ | C.②③④ | D.①②③④⑤ |
在复杂体系中,确认化学反应先后顺序有利于解决问题.下列反应先后顺序判断正确的是
| A.在含等物质的量的Fe2+、Ag+、Cu2+、H+的溶液中加入Zn: Ag+、Cu2+、H+、Fe2+ |
| B.在含等物质的量的AlO2-、OH-、CO32-溶液中,逐滴加入盐酸: AlO2-、Al(OH)3、OH-、CO32- |
| C.在含等物质的量的Ba(OH)2、KOH的溶液中通入CO2: KOH、Ba(OH)2、BaCO3 |
| D.在含等物质的量的FeBr2、FeI2的溶液中缓慢通入Cl2:I-、Br-、Fe2+ |
在一定条件下,对于反应mA(g)+n(B) cC(g)+dD(g),C的百分含量(C%)与温度、压强的关系如图所示,
cC(g)+dD(g),C的百分含量(C%)与温度、压强的关系如图所示,
下列该反应的 、
、 判断正确的是
判断正确的是
A. >0,
>0, <0 B.
<0 B. <0,
<0, >0
>0
C. >0,
>0, >0 D.
>0 D. <0,
<0, <0
<0
下列说法中正确的是
| A.6.8 g熔融KHSO4与3.9 g熔融Na2O2中阴离子数目相同 |
B.某金属阳离子的结构示意图为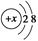 ,其与Cl-形成的强电解质都是离子化合物 ,其与Cl-形成的强电解质都是离子化合物 |
C.二硫化碳的电子式为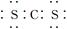 |
| D.中子数为18的氯原子可表示为18Cl |
设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.相同物质的量的OH-和CH3+含有相同数目的电子 |
| B.25℃时,pH=13的1.0 LBa(0H)2溶液中含有的OH-数目为0.2NA |
| C.标准状况下,2.24LCl2通入足量H2O或NaOH溶液中转移的电子数均为0.2NA |
| D.常温常压下,4.4gCO2和N2O混合物中所含有的原子数为0.3 NA |