常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表,请回答:
| 实验编号 |
HA物质的量浓度(mol·L-1) |
NaOH物质的量浓度(mol·L-1) |
混合溶液的pH |
| 甲 |
0.2 |
0.2 |
pH=a |
| 乙 |
c |
0.2 |
pH=7 |
| 丙 |
0.2 |
0.1 |
pH>7 |
| 丁 |
0.1 |
0.1 |
pH=9 |
(1)不考虑其它组的实验结果,单从甲组情况分析,如何用a (混合溶液的pH)来说明HA是强酸还是弱酸_________________________________________________________。
(2)不考虑其它组的实验结果,单从乙组情况分析,C是否一定等于0.2________(选填“是”或“否”)。
(3)丙组实验结果分析,HA是________酸(选填“强”或“弱”)。(4)丁组实验所得混合溶液中由水电离出的c(OH-)=________mol·L-1。
(4)写出该混合溶液中下式的精确结果(可写出算式,不能做近似计算):c(Na+)-c(A-)=________mol·L-1
研究CO2的利用对促进低碳社会的构建具有重要意义。
(1)将CO2与焦炭作用生成CO,CO可用于炼铁等。
已知:Fe2O3(s) + 3C(石墨) =" 2Fe(s)" + 3CO(g)△H 1 =" +489.0" kJ·mol-1
C(石墨) +CO2(g) = 2CO(g)△H 2 =" +172.5" kJ·mol-1
则CO还原Fe2O3(s)的热化学方程式为。
(2)二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式
CO2(g) +3H2(g) CH3OH(g) +H2O(g)△H
CH3OH(g) +H2O(g)△H
①该反应的平衡常数表达式为K=。
②取一定体积CO2和H2的混合气体(物质的量之比为1∶3),加入恒容密闭容器中,发生上述反应。反应过程中测得甲醇的体积分数φ(CH3OH)与反应温度T的关系如图A所示,则该反应的ΔH0(填“>”、“<”或“=”)。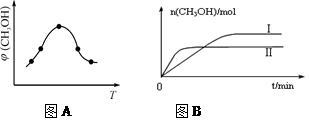
③在两种不同条件下发生反应,测得CH3OH的物质的量随时间变化如图B所示,曲线I、Ⅱ对应的平衡常数大小关系为KⅠKⅡ(填“>” 或“<”)。
(3)以CO2为原料还可以合成多种物质。①工业上尿素[CO(NH2)2]由CO2和NH3在一定条件下合成,其反应方程式为。当氨碳比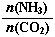 =3,达平衡时CO2的转化率为60%,则NH3的平衡转化率为。
=3,达平衡时CO2的转化率为60%,则NH3的平衡转化率为。
②用硫酸溶液作电解质进行电解,CO2在电极上可转化为甲烷,该电极反应的方程式为。
( 16分)Heck反应是合成C-C键的有效方法之一,如反应①: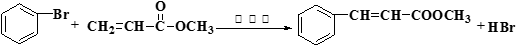
IⅡⅢ
化合物Ⅱ可由以下合成路线获得:
(1) 化合物Ⅲ的分子式为________,1 mol化合物Ⅲ完全燃烧最少需要消耗______mol O2。
(2)化合物IV分子结构中不含甲基,写出化合物IV的结构简式:______________,并写出由化合物IV反应生成化合物V的化学方程式___________________________。
(3)有关化合物Ⅱ说法正确的是_______________。
| A.1 mol 化合物Ⅱ最多可与2 mol H2发生加成反应 |
| B.化合物Ⅱ能使酸性高锰酸钾溶液褪色 |
| C.化合物Ⅱ难溶于水 |
D.化合物Ⅱ分子间聚合,反应生成的高聚物结构为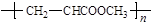 |
(4) 化合物Ⅲ的一种同分异构体VI,苯环上的一氯取代物只有一种,VI能发生银镜反应,其核磁共振氢谱共有三组峰,峰面积之比为1:2:2,VI的结构简式为_____________。
(5)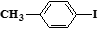 和
和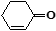 也可以发生类似反应①的反应,有机产物的结构简式_______________,①的反应类型为_____________。
也可以发生类似反应①的反应,有机产物的结构简式_______________,①的反应类型为_____________。
锂被誉为“金属味精”,以LiCoO2为正极材料的锂离子电池已被广泛用作便携式电源。工业上常以β-锂辉矿(主要成分为LiAlSi2O6,还含有FeO、MgO、CaO等杂质)为原料来制取金属锂。其中一种工艺流程如下:
已知:①部分金属氢氧化物开始沉淀和完全沉淀时的pH:
| 氢氧化物 |
Fe(OH)3 |
Al(OH)3 |
Mg(OH)2 |
| 开始沉淀pH |
2.7 |
3.7 |
9.6 |
| 完全沉淀pH |
3.7 |
4.7 |
11 |
②Li2CO3在不同温度下的溶解度如下表:
| 温度/℃ |
0 |
10 |
20 |
50 |
75 |
100 |
| Li2CO3的溶解度/g |
1.539 |
1.406 |
1.329 |
1.181 |
0.866 |
0.728 |
请回答下列问题:
(1)用氧化物形式表示LiAlSi2O6的组成:________________________。
(2)反应Ⅱ加入碳酸钙的作用是_________________________________。
(3)写出反应Ⅲ中生成沉淀A的离子方程式:______________________________________。
(4)反应Ⅳ生成Li2CO3沉淀,写出在实验室中得到Li2CO3沉淀的操作名称___________,洗涤所得Li2CO3沉淀要使用______________ (选填“热水”或“冷水”),你选择的理由是________________。
(5)电解熔融氯化锂生产锂时,阳极产生的氯气中会混有少量氧气,原因是:__________________________。
蓓萨罗丁是一种治疗顽固性皮肤T-细胞淋巴瘤的药物,有研究者设计其合成路线如下(部分反应试剂和条件已略):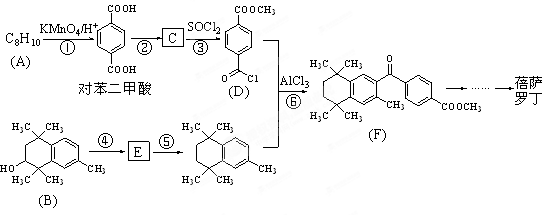
已知: 
试回答下列问题:
(1)A的结构简式为____________; F分子中含氧官能团的名称为_____________。
(2)D的分子式为_____________;原料B发生反应④所需的条件为____________________。
(3)反应①、⑥所属的反应类型分别为_____________ 、_________________。
(4)反应②、⑤的化学方程式分别为②______________;⑤ ____________________ 。
(5)对苯二甲酸有多种同分异构体,符合下列条件的同分异构体有__________种,写出其中任意一种的结构简式______________。①苯环上有三个取代基;②能与NaHCO3溶液发生反应;③能发生银镜反应。
已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D的合金是日常生活中常用的金属材料。常温常压下,E单质是淡黄色固体,常在火山口附近沉积。
(1)D在元素周期表中的位置为____________,C和E离子半径大小比较______________。
(2)A2E的燃烧热ΔH = -a kJ/mol,写出A2E燃烧反应的热化学方程式:_______________。
(3)CA的电子式为 ___________;AB形成的晶体熔点_______。(填“大于”“小于”或“无法判断”)CE形成的晶体熔点。
(4)甲、乙、丙分别是B、D、E三种元素最高价含氧酸的钠盐,甲、乙都能与丙发生反应,且丙用量不同,反应的产物不同。写出向丙溶液中缓慢滴加过量的乙溶液过程中反应的离子方程式:________ 。