下列选项中的反应类型与其他三个选项反应类型不同的是
A.CH2 = CH2+H2O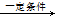 CH3CH2OH CH3CH2OH |
B.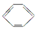 +HNO3 +HNO3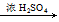 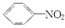 +H2O +H2O |
C.CH3COOH+CH3CH2OH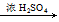 CH3COOCH2CH3+H2O CH3COOCH2CH3+H2O |
| D.CH3COOH+Cl2 → ClCH2COOH+HCl |
下列关于电解质溶液的叙述正确的是( )
| A.常温下,在pH=7的醋酸钠和醋酸混合溶液中:c(CH3COO-)>c(Na+) |
| B.稀释醋酸溶液,溶液中所有离子的浓度均降低 |
| C.在pH=5的氯化钠和稀硝酸的混合溶液中,c(Na+)=c(Cl-) |
| D.0.1mol•L-1的硫化钠溶液中,c(OH-)=c(H+)+c(HS-)+c(H2S) |
在25℃时,AgCl的白色悬浊液中,依次加入等浓度的KI溶液和Na2S溶液,观察到的现象是先出现黄色沉淀,最终出现黑色沉淀。已知有关物质的溶度积Ksp(25℃)如下:
| AgCl |
AgI |
Ag2S |
|
| Ksp |
1.8×10-10 |
8.51×10-16 |
6.3×10-50 |
下列叙述错误的是( )
A.沉淀转化的实质就是沉淀溶解平衡的移动
B.溶解度小的沉淀可以转化为溶解度更小的沉淀
C.AgCl固体在等物质的量浓度的NaCl、CaCl2溶液中的溶解程度相同
D.25℃时,在饱和AgCl、AgI、Ag2S溶液中,所含Ag+的浓度不同
下列水溶液一定呈中性的是( )
| A.c(NH4+)=c(Cl-)的NH4Cl和氨水的混合溶液 |
| B.c(H+)=1.0×10-7mol•L-1的溶液 |
| C.pH=7的溶液 |
| D.室温下将pH=3的酸与pH=11的碱等体积混合后的溶液 |
下列四种溶液中,水的电离程度最大的是( )
| A.pH=5的NH4Cl溶液 | B.pH=5的NaHSO4溶液 |
| C.pH=8的CH3COONa溶液 | D.pH=8的NaOH溶液 |
室温下,向10mL0.1 mol•L-1醋酸溶液中加水稀释后,下列说法正确的是( )
| A.溶液中导电粒子的数目减少 |
| B.再加CH3COONa固体促进醋酸的电离 |
| C.醋酸的电离程度增大,c(H+)亦增大 |
D.溶液中 不变 不变 |