【化学——选修:化学反应原理;必做题】
为有效控制雾霾,各地积极采取措施改善大气质量.有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要。
(1)在汽车排气管内安装催化转化器,可将汽车尾气中主要污染物转化为无毒的大气循环物质。
已知:①N2(g)+O2(g)=2NO(g)△H1=+180.5kJ/mol
②C和CO的燃烧热(△H)分别为-393.5kJ·mol-1和-283kJ·mol-1。
则2NO(g)+2CO(g)=N2(g)+2CO2(g)的△H=______________kJ·mol-1
(2)将0.20 molNO和0.10 molCO充入一个容积为1L的密闭容器中,反应过程中物质浓度变化如图所示。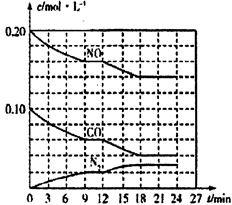
①0-9min内的平均反应速率v(N2)=_____mol· L-1·min-1(保留两位有效数字);第12 min时改变的反应条件可能为______________。
| A.升高温度 | B.加入NO | C.加催化剂 | D.降低温度 |
②该反应在第24 min时达到平衡状态,CO2的体积分数为__________(保留三位有效数字),化学平衡常数K=___________(保留两位有效数字)。
(3)烟气中的SO2可用某浓度NaOH溶液吸收得到Na2SO3和NaHSO3混合溶液,且所得溶液呈中性,该溶液中c(Na+)=____________(用含硫微粒浓度的代数式表示)。
(4)通过人工光合作用能将水与燃煤产生的CO2转化成HCOOH和O2.已知常温下0.1 mol·L-1的HCOONa溶液pH=10,则HCOOH的电离常数Ka=___________。
合理、高效利用金属矿物,将其中的金属从其化合物中还原出来用于生产和制造各种金属材料,这一过程在工业上称为金属的冶炼。
(1)以HgO为原料冶炼Hg,冶炼方法是。
(2)铝热法是冶炼金属的方法之一,写出铝热法炼铁(Fe2O3)的化学方程式:。引发铝热反应的实验操作是:
。
(3)某些金属氧化物粉末和铝粉在一定条件下可以发生铝热反应。下列反应速率(υ)和温度(T)的关系示意图中与铝热反应最接近的是:(填字母)。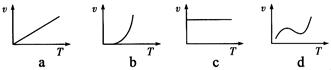
(10分) 莽草酸具有抗炎、镇痛作用,还可作为合成抗病毒和抗癌药物的中间体。莽草酸可以实现下列转化:
已知:①
请回答下列问题。
(1)A的结构简式是。
(2)B C的化学方程式是
C的化学方程式是
。
反应类型是反应。
(3)在有机物分子中,若碳原子连接四个不同的原子或原子团,该碳原予称为手性碳原
子。E分子中手性碳原子有个。
(4)莽草酸经过中间产物D合成E的目的是。
(10分) 化合物A经李比希法和质谱法分析得知其分子式是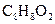 ,相对分子质量136。A的核磁共振氧谱有4个峰,峰面积之比为1:2:2:3,A分子中只含一个苯环且苯环上只有个取代基,其核磁共振氢谱与红外光谱如下图。
,相对分子质量136。A的核磁共振氧谱有4个峰,峰面积之比为1:2:2:3,A分子中只含一个苯环且苯环上只有个取代基,其核磁共振氢谱与红外光谱如下图。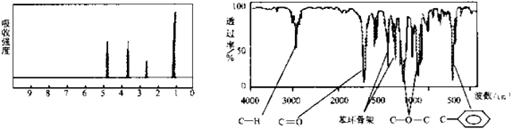
请回答下列问题。
(1)A的结构简式是。
(2)A的同分异构体(不含A) 中属于酯类的芳香族化台物共有种,请写出其
中任意两种的结构简式、。
(3)B与A互为同分异构体且能与碳酸氢钠反应,B的核磁共振氢谱也有4个峰,峰面
积之比为1:2:2:3,请参照示例写出以B和乙烯为原料在一定条件下台成聚酯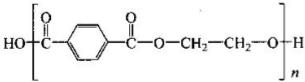 的合成路线。
的合成路线。
示例: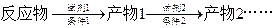
(10分) 肉桂酸是重要的有机合成中间体,广泛用于医药、香料、塑料和感光树脂等化工产品中。肉桂酸的结构简式为
请回答下列问题。
(1)肉桂酸的分子式是。
(2)写出肉桂酸的顺式结构。
(3)肉桂酸与乙醇在一定条件下发生反应的化学方程式是
。
(4)已知: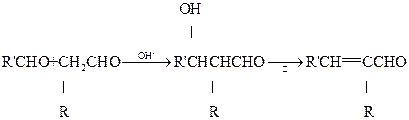
由苯甲醛制备肉桂酸的合成路线如下: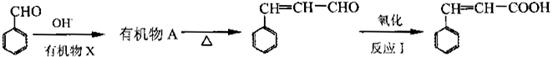
①上述合成路线中,反应I中氧化剂可选择(填写正确选项的字母)。
a.高锰酸钾酸性溶液 b.新制氧氧化铜 c.溴的四氯化碳溶液
②苯甲醛与有机物X反应生成A的化学方程式是
。
(8分) 某有机物A的相对分子质量为62。为进一步测定A的化学式,现取6.2 gA完全燃烧,得到二氧化碳和水蒸气。将产物先后通过足量的浓硫酸和碱石灰,两者分别增重
5.4 g和8.8 g (假设每步反应完全)。
(1)该有机物的实验式是:分子式是。
(2)红外光谱显示有“C—C”键和“O一H”键的振动吸收,若核磁兆振氢谱有2个吸收峰,峰面积之比为1:2,推断该有机物的结构简式是。
(3)该有机物与金属钠反应的化学方程式是。