我国某地利用生产磷铵排放的废渣磷石膏制取硫酸并联产水泥的技术研究获得成功。具体生产流程如下:
(1)操作a的名称是 。制硫酸工艺中净化SO2窑气的目的是 。
(2)装置B中生成两种酸式盐,它们的化学式分别是 。
(3)制硫酸所产生的尾气除了含有N2、O2外,还含有SO2、微量的SO3和酸雾。能用于测定硫酸尾气中SO2含量的是 。(选填字母)
| A.NaOH溶液、酚酞试液 | B.氨水、酚酞试液 |
| C.碘水、淀粉溶液 | D.KMnO4溶液、稀H2SO4液 |
(4)SO2可转化为硫酸盐。现有一种硫酸盐的化学式为Fe2(SO4)3·x(NH4)2SO4·yH2O。现称取该复盐2.410g,加入过量的NaOH溶液并加热,生成的气体用100mL 0.0500 mol·L―1硫酸吸收,多余的硫酸用0.2000 mol·L―1的NaOH溶液滴定,消耗NaOH溶液25.00mL。再将等质量的复盐溶于水配成溶液,加足量BaCl2溶液,充分反应后,过滤、洗涤、干燥,最后得白色沉淀2.330g。试列出计算过程确定该复盐的化学式。
实验室欲用NaNO3固体配制80 mL 1.4 mol·L-1的NaNO3溶液,试回答:
(1)用不到的仪器是__________;
A.烧杯B.500 mL容量瓶 C.量筒
D.胶头滴管 E.玻璃棒 F.100 mL容量瓶
(2)配制时应称取NaNO3__________g;
(3)实验开始时,需检查容量瓶__________;
(4)在配制一定物质的量浓度溶液的实验中,下列操作对所配溶液浓度无影响的是(写字母) __________;会使所配溶液浓度偏大的是__________;会使所配溶液浓度偏小的是__________。
A.在烧杯中溶解溶质,搅拌时不慎溅出少量溶液
B.未将洗涤烧杯内壁的溶液转移入容量瓶
C.容量瓶中所配的溶液液面未到刻度线便停止加水
D.将配得的溶液从容量瓶转移到干燥、洁净的试剂瓶中时,有少量溅出
E.将烧杯中溶液转移到容量瓶之前,容量瓶中有少量蒸馏水
F.容量瓶中液面将达到刻度线时,俯视刻度线和液面
乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物。完成下列各题: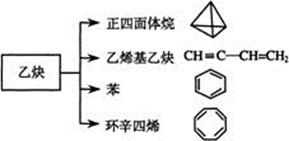
(1)正四面体烷的分子式为,其三氯取代产物有种
(2)关于乙烯基乙炔分子的说法正确的是:
a. 不能使酸性KMnO4溶液褪色
b. 等质量的乙炔与乙烯基乙炔完全燃烧时的耗氧量相同
c. 乙烯基乙炔分子中的四个C原子可能在一条直线上
d. 1摩尔乙烯基乙炔能与3摩尔Br2发生取代反应
(3)写出与苯互为同系物且一氯代物只有两种的物质的结构简式(举一例):。
(4)写出与环辛四烯互为同分异构体且属于芳香烃的分子的结构简式
某含C、H、O三种元素的未知A,经燃烧分析实验测定该未知物中碳的质量分数为52.16%,氢的质量分数为13.14%。
(1)该未知物A的实验式为。能否直接依据A的实验式确定A的分子式。(填“能”或“否”)
(2)A物质在浓硫酸和170℃的条件下生成一种化工原料B,写出B物质在催化剂的条件下生成高分子化合物的化学方程式。
(一)某烯烃与H2发生加成反应后得到的产物是CH3—CH(CH3)2.
⑴原来烯烃的名称是
⑵ 原来烯烃的结构简式为:
⑶ 写出原来的烯烃使溴的四氯化碳溶液褪色的化学反应方程式:
(二)某烷烃碳架结构如图所示: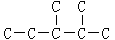 ,
,
(1)此烷烃的一溴代物有种
(2)若此烷烃为炔烃加氢制得,则此炔烃的结构简式为
(3)若此烷烃为单烯烃加氢制得,则此烯烃的结构有种
(1)有机物CH3CH(C2H5)CH(C2H5)CH(CH3)2按系统命名法命名的名称是
(2) 卤代烃C5H11Cl中含有2个-CH3的同分异构体有种
(3) 已知乙炔(C2H2)、苯(C6H6)、乙醛(C2H4O)的混合气体中含氧元素的质量分数为8%,则混合气体中碳元素的质量分数为