雄黄(As4S4)和雌黄(As2S3)是提取砷的主要矿物原料,二者在自然界中共生。根据题意完成下列填空:
(1)As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体。若As2S3和SnCl2正好完全反应,As2S3和SnCl2的物质的量之比为 。
(2)As2S3和HNO3有如下反应,As2S3+10H++ 10NO3—="2H3AsO4+" 3S+10NO2↑+ 2H2O
若生成2mol H3AsO4,则反应中转移电子的物质的量为 。若将该反应设计成一原电池,则NO2应该在 (填“正极”或“负极”)附近逸出。
(3)若反应产物NO2与11.2L O2(标准状况)混合后用水吸收全部转化成浓HNO3,然后与过量的碳反应,所产生的CO2的量 (选填编号)。
a.小于0.5 mol b.等于0.5mol c.大于0.5mol d.无法确定
某反应中反应物与生成物有:AsH3、H2S04、KBr03、K2SO4、H3AsO4、H20和一种
未知物质X。
(1)已知KBrO3在反应中得到电子,则该反应的还原剂是
(2)已知O.2molKBrO3在反应中得到1 mol电子生成X.则X的化学式为。
(3)根据上述反应可推知。
a.氧化性:KBrO 3> H3AsO4
3> H3AsO4
b.氧化性:H3AsO4>KBr03
c.还原性:AsH3>X
d.还原性:X>AsH3
(4)组合并配平有上述物质参加和生成的反应化学方程式:

2008年11月1 日上午lO时许,在镇江支路12号青岛亨通达实业有限公司热电厂院内,8 231.25公斤含有三聚氰胺(结构简式为: )的乳制品在工商、质监等部门的监管下,和煤炭掺搅在一起填炉焚烧销毁.
)的乳制品在工商、质监等部门的监管下,和煤炭掺搅在一起填炉焚烧销毁.
根据上述信息,回答下列问题:
(1)三聚氰胺属于.
A.铵盐 B.高分子化合物 C.有机物 D.蛋白质
(2)下列属于纯净物的是.
A.煤炭 B.三聚氰胺 C.不含三聚氰胺的奶粉 D.聚乙烯
(3)奶粉中含有蛋白质,溶于水后形成的分散系称为,若用一束光照射该分散系,会发现.
(4)三聚氰胺的化学式是,其中氮元素的质量分数为,不法商人及企业在奶粉及牛奶中掺入三聚氰胺的目的是
向Ba(OH)2溶液中逐滴加入稀硫酸,请完成下列问题:
(1)写出反应的离子方程式:
(2)下列三种情况下,离子方程式与(1)相同的是(填序号)。
A.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性
B.向NaHS04溶液中.逐滴加入Ba(OH)2溶液至SO42-恰好完全沉淀
C.向NaHS04溶液中,逐滴加入Ba(OH)2溶液至过量
(3)若缓缓加入稀硫酸直至过量,整个过程中混合溶液的导电能力(用电流强度I表示)可近似地用如图中的 (填序号)曲线表示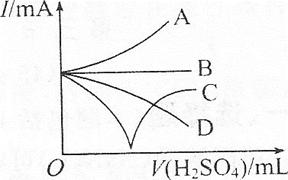
(4)若有一表面光滑的塑料小球悬浮于Ba(OH)2溶液中央,如图所示,向该烧杯里缓缓注入与Ba(OH)2溶液等密度的稀硫酸至恰好完全反应。在此实验过程中,小球将。
指出下列哪些是碳链异构___________;哪些是位置异构______________;哪些是官能团异构_____________。
| A.CH3CH2COOH | B.CH3-CH(CH3)-CH3 | C.CH2=CH-CH=CH2 | D.CH3COOCH3 E.CH3-CH2-C≡CH F.HCOOCH2CH3 |
G.CH3C≡CCH3H.CH3-CH2-CH2-CH3
请同学们根据官能团的不同对下列有机物进行分类。
(1)芳香烃:;(2)卤代烃:;
(3)醇:;(4)酚:;
(5)醛:;(6)酮:;
(7)羧酸:;(8)酯:。