在25℃时,将酸HA与碱MOH等体积混合.
(1)若0.01mol/L的强酸HA与0.01mol/L强碱MOH混合,则所得溶液显 (填“酸性”、“中性”或“碱性”,下同)该反应的离子方程式为 。
(2)若PH=3的强酸HA与PH=11的弱碱MOH混合,则所得溶液显 ,
理由是 。
(3)若0.01mol/L的强酸HA与0.01mol/L弱碱MOH混合,则所得溶液显 ,解释这一现象的离子方程式是 。
湿法炼锌的冶炼过程可用下图简略表示:
请回答下列问题:
(1)已知:N2(g)+2H2(g)===N2H4(l) ΔH=a kJ·mol-1,该反应不能自发进行,则a0(填“>”、“<”或“=”).
(2)ZnS焙烧的反应2ZnS+3O2 2SO2+2ZnO所涉及的物质中,发生氧化反应的物质是,不含离子键的化合物是.
2SO2+2ZnO所涉及的物质中,发生氧化反应的物质是,不含离子键的化合物是.
(3)电解过程中析出锌的电极反应式为___________________________.
(4)产生的SO2可用Ba(NO3)2溶液吸收,部分产物可作为工业原料,其反应的离子方程式为.
(5)锌-空气电池与锂电池相比,具有储存电量高、成本低、没有安全隐患等优点。该电池的总反应为2Zn+O2===2ZnO,电解质溶液为KOH溶液,则负极的电极反应式为。25℃时,以该电池为电源,用两个等质量的铜棒作电极电解500 mL 0.1mol/L CuSO4溶液,一段时间后切断电源,对电极干燥并称量,测得两电极的质量差为9.6 g,则至少需要________L空气(折算成标准状况)进入该电池。
Ⅰ 某药物中间体A的分子式为C9H8O4,在一定条件下能与醇发生酯化反应,其红外光谱表明苯环上的两个取代基连接在对位碳原子上。D能与NaOH溶液反应但不能与NaHCO3溶液反应。A的相关转化如下图所示: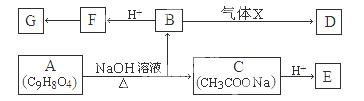
回答下列问题:
(1)A转化为B、C所涉及的反应类型是、.
(2)反应B→D的化学方程式是.
(3)同时符合下列要求的F的同分异构体有种,其中一种同分异构体的结构简式为.
①属于芳香族化合物; ②能发生银镜反应,不能发生水解反应;③在稀KOH溶液中,1 mol 该同分异构体能消耗2 mol KOH;④一氯代物只有两种.
(4)G为高分子化合物,其结构简式是.
(5)化合物D有如下转化关系: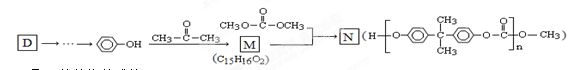
①M的结构简式为.
②N与足量NaOH溶液共热的化学方程式为.
元素及其化合物在生产、生活中具有广泛的用途。
Ⅰ.铬化学丰富多彩:
⑴在常温下,铬能缓慢与稀硫酸反应,生成蓝色溶液。与铜相比,其金属活泼性。(填“强”或“弱”)
⑵Cr( OH)3和Al( OH)3类似,也是两性氢氧化物,在水中存在酸式和碱式电离平衡,其酸式电离方程式是。
(3)工业上净化处理铬污染方法之一:将含K2Cr2O7酸性废水放入电解槽内,加入适量的NaCl,以Fe和石墨为电极进行电解。一段时间后,生成Cr(OH)3和Fe(OH)3沉淀除去(已知Ksp[ Fe(OH)3]=4.0×10-38,Ksp[Cr(OH)3]=6.0×l0-31)。已知电解后的溶液中c( Fe3+)为2.0×10-13mol/L,则溶液中c(Cr3+)为 mol/L。
Ⅱ.物质A~H有如图所示转化关系(部分生成物未列出)。A、E、F、G均为气体,D为贵重金属之一。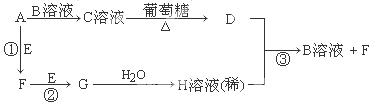
请回答下列问题:
(1)A分子是分子(填“极性”或“非极性”),C溶液中的阳离子是(写化学式,不考虑水的电离)。
(2)反应①的化学方程式为;反应③的离子方程式为。
(15分) 化合物A和B都是重要的化工原料。B和E都能与FeCl3溶液发生显色反应,B、C、D结构中都有两个化学环境完全相同的甲基,B中苯环上的一硝基取代物只有两种。X是石油裂解的主要产物,通过质谱法测得其相对分子质量为42。
已知:
请回答下列问题:
(1)下列叙述正确的是______。
a.化合物Y能使酸性高锰酸钾溶液褪色
b.化合物X的结构简式为CH2=CHCH3
c.化合物C、D互为同系物
d.A与NaOH溶液反应,理论上1 mol A最多消耗2 mol NaOH
(2)X→Y的反应类型是______,化合物B的结构简式是________,化合物C的结构简式是________。
(3)写出Y→D + E的化学方程式____________________________。
(4)写出同时满足下列条件的B的两种同分异构体的结构简式(不考虑立体异构)。
a.有两个化学环境相同的甲基,含稠环芳烃的结构单元
b.苯环上的一硝基取代物只有两种,遇FeCl3溶液显色
(5)以X和甲醛为原料合成化合物C,请设计合成路线(无机试剂及溶剂任选)。
注:合成路线参照如下示例流程图:
二甲醚(DME)和甲醇是21世纪应用最广泛的两种清洁燃料,目前工业上均可由合成气在特定催化剂作用下制得。
(1)由合成气制备二甲醚的主要原理如下:
已知:①CO(g)+2H2(g) CH3OH(g) △H1=-90.7 kJ·mol-1
CH3OH(g) △H1=-90.7 kJ·mol-1
②2CH3OH(g) CH3OCH3(g)+H2O(g) △H2=-23.5 kJ·mol-1
CH3OCH3(g)+H2O(g) △H2=-23.5 kJ·mol-1
③CO(g)+H2O(g) CO2(g)+H2(g) △H3=-41.2 kJ·mol-1
CO2(g)+H2(g) △H3=-41.2 kJ·mol-1
则反应3H2(g)+3CO(g) CH3OCH3(g)+CO2(g)的△H=kJ·mol-1。
CH3OCH3(g)+CO2(g)的△H=kJ·mol-1。
(2)将合成气以n(H2)/n(CO)=2通入1 L的反应器中,一定条件下发生反应:
4H2(g)+2CO(g) CH3OCH3(g)+H2O(g),其中CO的平衡转化率随温度、压强变化关系如图所示:
CH3OCH3(g)+H2O(g),其中CO的平衡转化率随温度、压强变化关系如图所示:
①该反应的平衡常数表达式为;P1、P2、P3由大到小的顺序为。
②若反应在P3和316℃时,起始时n(H2)/n(CO)=3,则达到平衡时,CO的转化率50%(填“大于”、“小于”或“等于”)。
(3)由合成气合成甲醇的反应的温度与平衡常数(K)的关系如表数据,

250℃时,将2 molCO和6 molH2充入2L的密闭容器中发生反应,反应时间与物质浓度的关系如图所示,则前10分钟内,氢气的平均反应速率为;若15分钟时,只改变温度一个条件,假设在20分钟时达到新平衡,氢气的转化率为33.3%,此时温度为(从上表中选),请在图中画出15—25分钟c (CH3OH)的变化曲线。
(4)利用甲醇液相脱水也可制备二甲醚,原理是:CH3OH +H2SO4→CH3HSO4+H2O,CH3HSO4+CH3OH→CH3OCH3+H2SO4。与合成气制备二甲醚比较,该工艺的优点是反应温度低,转化率高,其缺点是。