下列各组离子在碱性条件下能大量共存,而在强酸性条件下也能发生氧化还原反应的是
| A.Mg2+、Na+、SO42-、Cl- | B.K+、CO32-、Cl-、NO3- |
| C.Na+、K+、NO3-、SO32- | D.NH4+、Na+、SO42-、NO3- |
下列依据热化学方程式得出的结论正确的是()
A.已知2H2(g)+O2(g) 2H2O(g) ΔH =-483.6 kJ·mol–1,则氢气的燃烧热为241.8 kJ·mol–1 2H2O(g) ΔH =-483.6 kJ·mol–1,则氢气的燃烧热为241.8 kJ·mol–1 |
B.已知C(石墨,s) C(金刚石,s) ΔH>0,则石墨比金刚石稳定 C(金刚石,s) ΔH>0,则石墨比金刚石稳定 |
C.已知OH–(aq)+H+(aq) H2O(l) ΔH=-57.4 kJ·mol–1,则含20.0 g NaOH的稀溶液与CH3COOH的稀溶液完全中和,放出的热量等于28.7 kJ H2O(l) ΔH=-57.4 kJ·mol–1,则含20.0 g NaOH的稀溶液与CH3COOH的稀溶液完全中和,放出的热量等于28.7 kJ |
D.已知2C(s)+2O2(g) 2CO2(g) ΔH1 2C(s)+O2(g) 2CO2(g) ΔH1 2C(s)+O2(g) 2CO(g) ΔH2,则ΔH1>ΔH2 2CO(g) ΔH2,则ΔH1>ΔH2 |
关于下列各装置图的叙述中,正确的是()
| A.若采用装置①精炼铜,则a极为纯铜, b极为粗铜,电解质溶液为CuSO4溶液 |
| B.装置②是原电池,能将化学能转化为电能,锌电极发生还原反应 |
| C.装置③中X若为四氯化碳,则此装置可用于吸收氨气,并防止倒吸 |
| D.装置④可用于实验室配制一定物质的量浓度的稀硫酸 |
阿伏加德罗常数的值约为6.02×1023,下列说法正确的是()
A.l.8 g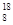 O2分子与1.8 g O2分子与1.8 g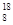 O3分子中含有的中子数不相同 O3分子中含有的中子数不相同 |
| B.标准状况下,22.4LCCl4中共价键数为4NA |
| C.80 mL 10 mol·L–1浓盐酸与足量MnO2反应,转移电子数为0.4×6.02×1023 |
| D.常温常压下,6.02×1023个SO3分子所占的质量约为80 g |
下列实验方案能达到预期目的的是()
①实验室保存FeCl3溶液应加少量稀盐酸,并且放入少量的Fe粉
②氢氧化钠溶液保存在配有橡胶塞的细口瓶中
③向溶液中滴入氯化钡溶液,再加稀硝酸能检验溶液中是否含有SO
④用丁达尔现象可以区分食盐水和淀粉溶液
⑤工业上可用金属铝与V2O5在高温下冶炼V(钒),铝作还原剂
| A.②④⑤ | B.①②⑤ | C.①②④ | D.②③④ |