氯气是一种重要的工业原料。
(1)实验室可用高锰酸钾和浓盐酸反应制取氯气,反应的化学方程式是:
_______________________________________________________________________。
(2)资料显示:Ca(ClO)2+CaCl2+2H2SO4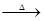 2CaSO4+2Cl2↑+2H2O。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质:
2CaSO4+2Cl2↑+2H2O。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质:
①在该实验中,甲部分的装置是__________(填字母)。
如何检查该装置的气密性?______________________________________________。
②乙装置中FeCl2溶液与Cl2:反应的离子方程式是_______________。
③丙装置中通人少量Cl2,可制得某种生活中常用的漂白、消毒的物质。已知碳酸的酸性强于次氯酸.则丙中发生反应的化学方程式是____________。
④该实验存在明显的缺陷.改进的方法是________________________________________________。
除去下列物质中所含的杂质,将除杂质试剂和操作方法填入空格。
| 物质 |
杂质 |
除杂试剂 |
操作方法 |
|
| 1) |
苯 |
苯酚 |
||
| 2) |
乙炔 |
硫化氢 |
||
| 3) |
溴苯 |
溴 |
||
| 4) |
柴油 |
汽油 |
_____________ |
实验室制取乙烯的装置如右图所示,请根据图示回答下列问题: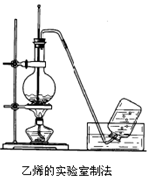
(1)该反应类型属于_________________________;
实验室制乙烯的化学方程式为_________________________________________________
(2)某化学课外兴趣小组学生在实验室里制取的乙烯中常混有少量的二氧化硫,老师启
发他们并由他们自己设计了下列实验图以确认上述混合气体中有C2H4和SO2。回答下列
问题: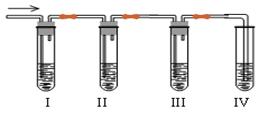
①、I、II、Ⅲ、IV装置可盛放的试剂是IIIⅢIV____(填试剂的序号)。
| A.品红溶液 | B.NaOH溶液 | C.浓硫酸 | D.酸性KMnO4溶液 |
②、能说明SO2气体存在的现象是_____________________________________________。
③、使用装置II的目的是_____________________________________________________。
④、使用装置Ⅲ的目的是_____________________________________________________。
⑤、确定含有乙烯的现象是____________________________________________________
几位同学设计实验观察铜与浓硫酸的反应,检验生成的气体的性质。甲设计了如图所示的装置,在大试管里加入2mL浓硫酸,用带导管和一个小孔的胶管塞紧,从孔中插入一根铜丝,加热,把产生的气体依次通入品红溶液和石蕊溶液中。
请回答下列问题:
(1)写出铜与浓硫酸反应的化学方程式:。
(2)试管b中的现象是,
通过试管a、b的现象得出的结论是。
(3)乙同学认为甲同学的设计不能全面体现SO2的性质,他打算增加试管进行其它实验。以下为增加的试管中盛放的试剂:A. 澄清石灰水 B. KMnO4(aq) C. 氢硫酸
请你帮助乙同学作出选择,在横线上先写出字母,再用文字简单说明实验的目的。
(4)丙同学评价甲同学的实验装置既有优点也有不足,优点是
,不足之处改进的具体措施是。
(5)若把上述装置中大试管的浓硫酸换成稀硝酸,试管a和b作如下改变(其中a装满水,b空置),则在大试管中发生的反应的离子方程式为,
试管a的作用是。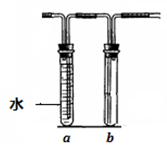
某同学做同周期元素性质递变规律实验时,设计了一套实验方案,并记录了有关实验现象(见下表,表中左右的“实验方案”与“实验现象”不一定是对应关系)。
| 实验方案 |
实验现象 |
| ①镁条除去氧化膜后,放入试管中,加入少量水,加热至沸腾;再向溶液中滴加酚酞溶液 |
A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变红色 |
| ②向新制得的Na2S溶液中滴加新制的氯水 |
B.有气体产生,溶液变成浅红色 |
| ③将小块金属钠放入滴有酚酞溶液的冷水中 |
C.剧烈反应,迅速产生大量无色气体 |
| ④将除去氧化膜的镁条投入稀盐酸中 |
D.反应不十分剧烈,产生无色气体 |
| ⑤将除去氧化膜的铝条投入稀盐酸中 |
E.生成白色胶状沉淀,继而沉淀消失 |
| ⑥向A1Cl3溶液中滴加NaOH溶液至过量 |
F.生成淡黄色沉淀 |
请你帮助该同学整理并完成实验报告。
(1)实验目的:研究第3周期元素性质的递变规律。
(2)实验用品:
试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液,AlCl3溶液,NaOH
溶液,酚酞溶液等。
仪器:砂纸,试管,试管夹,①,火柴,胶头滴管,烧杯,镊子,小刀,玻璃片,
②等。
(3)实验内容:
| 实验方案 |
② |
④ |
⑥ |
| 实验现象(填A~F) |
①的化学方程式,
②的离子方程式。
(4)实验结论:。
某研究小组探究SO2和Fe(NO3)3溶液的反应。
已知: 1.0 mol/L的Fe(NO3)3溶液中c(H+)=0.01mol/L
请回答:
(1)装置A中反应的化学方程式是。
(2)为排除空气对实验的干扰,滴加浓硫酸之前应进行的操作是。
(3)装置B中产生了白色沉淀,其成分是,说明SO2具有性。
(4)分析B中产生上述白色沉淀的原因可能是:
观点1:;
观点2:SO2与Fe3+反应;
观点3:在酸性条件下SO2与NO3-反应;
①如果观点2正确,装置B中反应的离子方程式是
②如果想验证观点3,只需将装置B中的 Fe(NO3)3溶液替换为等体积的下列溶液,在相同条件下进行实验。应选择的试剂是(填序号)。
a.0.1 mol/L 稀硝酸
b.1.5 mol/L Fe(NO3)2溶液
c.6.0 mol/L NaNO3和0.02 mol/L盐酸等体积混合的溶液