设NA为阿伏加德罗常数,下列叙述正确的是
| A.18g水中所含的电子数为8NA |
| B.11.2L氯气所含的分子数为0.5NA |
| C.2.4gMg与足量的盐酸反应失去的电子数为0.2NA |
| D.32g氧气中所含的氧原子数为N |
下列离子的检验方法合理的是
| A.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- |
| B.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ |
| C.用铂丝蘸取少量固体,置于酒精灯火焰上灼烧,若有黄色火焰产生,该固体中一定含Na+,不含K+。 |
| D.验证烧碱溶液中是否含有Cl-,先加稀硝酸除去OH-,再加入AgNO3溶液,有白色沉淀,证明有Cl- |
将NO2和NH3混合,在一定条件下发生反应: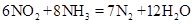 ,下列说法正确的是
,下列说法正确的是
| A.NO2被氧化 | B.NO2既是氧化剂,又是还原剂 |
| C.NO2是氧化剂 | D.1 mol NH3反应,转移3mol电子 |
不能用来鉴别Na2CO3和NaHCO3两种白色固体的实验操作是
| A.分别加热这两种固体物质,并将生成的气体通入澄清的石灰水中 |
| B.分别在这两种物质的溶液中加入CaCl2溶液 |
| C.分别在这两种固体中加入同浓度的稀盐酸 |
| D.分别在这两种物质的溶液中加入少量澄清的石灰水 |
过滤后的食盐水仍含有可溶性的CaCl2、MgCl2、Na2SO4等杂质,通过如下几个实验步骤,可制得纯净的食盐水:① 加入稍过量的Na2CO3溶液;② 加入稍过量的NaOH溶液;③ 加入稍过量的BaCl2 溶液;④滴入稀盐酸至无气泡产生;⑤ 过滤。正确的操作顺序是
| A.①②③⑤④ | B.③②①⑤④ | C.②③①⑤④ | D.③⑤②①④ |
用NA表示阿伏加德罗常数,下列叙述正确的是
| A.标准状况下,22.4L H2O含有的分子数为1 NA |
| B.通常状况下,1 NA个CO2分子占有的体积为22.4L |
| C.常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA |
| D.物质的量浓度为0.5mol/L的Mg(NO3)2溶液中,含有NO3-个数为1 NA |