(14)CO2是最重要温室气体,如何降低大气中CO2的含量及有效地开发利用CO2具有重大意义。
(1)科学家用H2和CO2生产甲醇燃料。为探究该反应原理,进行如下实验:某温度下,在容积为2 L的密闭容器中充入1 mol CO2和3.5 mol H2,在一定条件下反应,测得CO2、CH3OH(g)和H2O(g)的物质的量(n)随时间的变化关系如图所示。
①写出该反应的化学方程式_______________________计算从反应开始到3 min时,氢气的平均反应速率v(H2)=____________________。
②下列措施中一定能使CO2的转化率增大的是___________________ 。(双选、填序号)
| A.在原容器中再充入1 mol H2 | B.在原容器中再充入1 mol CO2 |
| C.缩小容器的容积 | D.使用更有效的催化剂 |
(2)科学家还利用氢气在一定条件下与二氧化碳反应生成乙醇燃料,其热化学反应方程式为:
2CO2(g)+6H2(g) CH3CH2OH(g)+3H2O(g) ΔH=a kJ·mol-1,
CH3CH2OH(g)+3H2O(g) ΔH=a kJ·mol-1,
在一定压强下,测得该反应的实验数据如表所示。请根据表中数据回答下列问题。
①上述反应的a________0(填“大于”或“小于”)。
②恒温下,向反应体系中加入固体催化剂,则该反应的反应热a值____(填“增大”、“减小”或“不变”)。
在一定温度下,增大 的值,CO2转化率_________,生成乙醇的物质的量________(填“增大”、“减小”、“不变”或“不能确定”)。
的值,CO2转化率_________,生成乙醇的物质的量________(填“增大”、“减小”、“不变”或“不能确定”)。
写出下列有机化学反应方程式,并指出反应类型:
(1)写出乙烯使溴水退色的化学方程式________________________________,该反应属于________反应。
(2)写出乙烯在催化剂作用下生成聚乙烯的化学反应方程式,该反应属于_______反应。
(3)实验室制取乙烯的反应,该反应属于反应。
⑷乙醛在一定温度和催化剂作用下氧化成乙酸的化学反应方程式
_____________________________,该反应属于反应。
⑸写出乙醇与浓氢溴酸的混合加热发生反应的化学方程式
________________________________________,该反应属于反应。
决定有机化合物化学性质的原子或原子团叫做官能团,如卤原子(—X),氨基(—NH2),碳碳叁键(—C≡C—)等。
(1)乙醛能起银镜反应,说明乙醛分子中含有(写名称)官能团。
(2)水杨酸的结构简式为: ,其有种官能团。
,其有种官能团。
为了达到下列表格中的实验要求,请从供选择的化学试剂及实验方法中选出合适的,将其标号填入对应的空格中。
| 实验要求 |
试剂及方法 |
| 证明明矾水溶液呈酸性 |
|
| 鉴别甲烷与乙烯 |
|
| 除去MgO中含有的Al2O3 |
|
| 鉴别乙醇和乙醛 |
供选择的化学试剂及实验方法
A.新制的Cu(OH)2
B.加盐酸,过滤
C.将溶液滴在pH试纸上
D.加入过量浓NaOH溶液,过滤
E.酸性KMnO4溶液
用于提纯或分离物质的方法有:
| A.萃取分液; | B.加热分解; | C.蒸发结晶; | D.分液;E、蒸馏;F、过滤等,请将提纯或分离方法的序号填在后面横线上。 |
(1)从碘水里提取碘___________
(2)分离水和汽油的混合物___
(3)分离相溶的CCl4(沸点:76.75℃)和甲苯(沸点:110.6℃)的混合物_____
在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命。
(1)现有一种无色的鲜花营养液,可能由硝酸钙、碳酸钾、硝酸钾、氯化钾中的一种或几种物质组成,为探究其成分,某同学设计并完成了如下图所示的实验。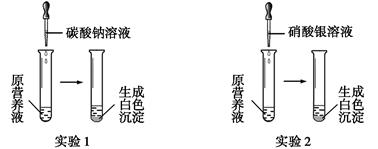
根据以上实验,请你填空。
①由实验1可确定原营养液中一定没有的物质是(填化学式),写出生成白色沉淀的离子方程式是。
②若测得原营养液中K+、Cl-的数目之比为2∶1,则原营养液是由种溶质配制成的。
③某同学用氯化钙、硝酸钾、氯化钾配成的营养液中K+、Cl-、NO3-的数目之比为2∶5∶1,
则所用硝酸钾和氯化钙的物质的量之比是。
(2)下表是500mL某“鲜花保鲜剂”中含有的成分,阅读后回答下列问题。
| 成分 |
质量(g) |
摩尔质量(g ·mol-1) |
| 蔗糖 |
68.4 |
342 |
| 硫酸钾 |
0.50 |
174 |
| 阿司匹林 |
0.35 |
180 |
| 高锰酸钾 |
0.50 |
158 |
| 硝酸银 |
0.04 |
170 |
①“鲜花保鲜剂”中蔗糖的物质的量浓度为___________________。
②配制该500mL “鲜花保鲜剂”所需的玻璃仪器除了烧杯、玻璃棒、量筒外还有。
③在溶液配制过程中,下列操作能使配制结果偏小的是___________。
A.定容时仰视容量瓶刻度线
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.移液时,液体不小心从外壁流出
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理