(12分,每空2分)
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。请回答:
(1)在一定体积的恒容密闭容器中,进行如下化学反应:
N2(g)+3H2(g) ⇌2NH3(g);△H<0
其化学平衡常数K与温度t的关系如下表,根据下表完成下列问题:
| t/K |
298 |
398 |
498 |
… |
| K/(mol·L-1)2 |
4.1×106 |
K1 |
K2 |
… |
①比较K1、K2的大小:K1 K2(填“>”、“=”或“<”)。
②判断该反应达到化学平衡状态的依据是 (填序号)。
A.2v(H2)(正)=3v(NH3)(逆)
B.混合气体中氢气的质量不变
C.容器内压强保持不变
D.混合气体的密度保持不变
③某温度下,在一个10L的固定容器中充入2molN2和4molH2进行如下反应 N2(g)+3H2(g) ⇌2NH3(g);△H<0一段时间达平衡后,N2的转化率为50%,求该温度下的平衡常数K= (mol/L)-2 ,平衡时NH3的体积分数为 。
(2)①肼(N2H4)高效清洁的火箭燃料。8g气态肼在氧气中完全燃烧生成氮气和气态水,放出133.5kJ热量,则肼燃烧的热化学方程式为 。
②盐酸肼(N2H6Cl2)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,则盐酸肼中含有的化学键类型有 。
(1)将锌片和银片浸入稀硫酸中组成原电池,两电极间连接一个电流计。锌片上发生的电极反应:;银片上发生的电极反应:。
(2)若该电池中两电极的总质量为60g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47g,试计算:产生氢气的体积(标准状况)。
(10分,每空2分)按要求填下列物质。
(1)分子中含有14个氢原子的烷烃的名称是。
(2)相对分子质量为44的烷烃的分子式为。
(3)碳、氢原子个数比为2:5的烷烃分子式为,它的同分异构体的结构简式为。
(4)含碳质量分数约为75%的烷烃的结构式为。
(6分,每空2分)下图表示的是在800℃时,含有A、B、C三种气体的体系中各物质浓度随时间变化的情况,请回答: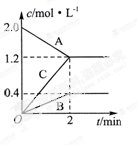
(1)该反应的反应物是。
(2)该反应的化学方程式是。
(3)若达到平衡状态的时间为2min,则A物质的平均反应速率为。
(4分,每空1分)如图所示,把试管放入盛有25℃饱和石灰水的烧杯中,试管中开始放入几小片镁片,再用滴管滴5mL稀盐酸于试管中。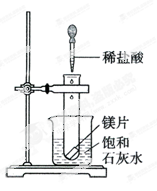
试回答下列问题:
(1)实验中观察到的现象是。
(2)产生上述现象的原因是。
(3)写出有关反应的离子方程式:。
(4)由实验推知,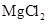 溶液和氢气的总能量(填“大于”“小于”或“等于”)镁片和稀盐酸的总能量。
溶液和氢气的总能量(填“大于”“小于”或“等于”)镁片和稀盐酸的总能量。
A、B、C为短周期元素,在周期表中所处的位置如图所示。A、C两元素的原子核外电子数之和等于B原子的质子数,B原子核内质子数和中子数相等。
| A |
C |
|
| B |
(1)A、B、C三种元素的名称分别为、、。
(2)B位于元素周期表中第周期、第族。
(3)C的原子结构示意图为,C的单质与 反应的化学方
反应的化学方
程式为。
(4)写出A的气态氢化物与B的最高价氧化物对应水化物反应的化学方程式。