在500℃时,将足量的A固体投入2.0L真空密闭容器中,发生A(s)  2B(g)+C(g)反应,测得气体C随时间的浓度变化如图所示
2B(g)+C(g)反应,测得气体C随时间的浓度变化如图所示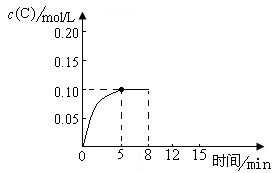
(1)已知该反应只有高温下能自发进行,则该反应的△H 0(填“>”、“<”或“=”)。
(2)在上述反应条件下,从反应开始到平衡,用V(B)= mol·L-1·min-1,500℃时的平衡常数K= ;
(3)在反应温度和容器体积不变的条件下,下列能说明上述反应达到平衡状态的是 ;
A.混合气体的压强保持不变
B.气体C的体积分数保持不变
C.混合气体的密度保持不变
D.B的正反应速率等于C的逆反应速率
(4)在500℃时,上述反应达到平衡后,在8min时将容器体积迅速压缩为1.0L,反应在12min建立新的平衡,画出8~15min内C气体物质的量浓度随时间变化的示意图。
香豆素类化合物具有抗病毒、抗癌等多种生物活性。香豆素-3-羧酸可由水杨醛制备。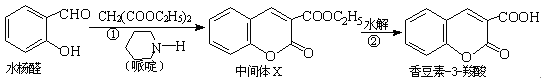
(1)水杨醛的核磁共振氢谱有______个峰。
(2)中间体X含有的官能团名称为。
(3)下列说法错误的是()(单选)
| A.中间体X不易溶于水 |
| B.1 mol 香豆素-3-羧酸最多可以与5 mol H2加成 |
| C.香豆素-3-羧酸可以与NaHCO3溶液反应放出CO2 |
| D.水杨醛和香豆素-3-羧酸都能使酸性高锰酸钾溶液褪色 |
(4)水杨醛有多种同分异构体,写出其中一种既可以发生银镜反应,又可以发生水解反应的结构简式:。
(5)香豆素-3-羧酸与足量NaOH溶液加热发生反应的化学方程式为:。
(6)反应①中的催化剂“哌啶”可以由“吡啶”合成,其反应为:
已知吡啶为环状,性质与苯类似。则吡啶的结构简式为;吡啶与混酸(浓硝酸与浓硫酸混合物)在加热条件下,发生硝化反应生成氮原子间位的一取代物的化学方程式为。
回答下列问题:
(1)用乙炔制备聚氯乙烯( )(自行选择无机原料),
)(自行选择无机原料),
请书写化学反应方程式:_______;________。
(2实验室用乙醇制乙烯的反应方程式为________。其反应类型为________。检验生成的乙烯要将导管先后通入______、_________。(填试剂名称)
(3)由溴乙烷为原料合成1,2-二溴乙烷(自行选择无机原料),
请书写化学反应方程式:_______;________。
(4)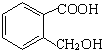 能发生反应生成一种含五元环的化合物,请书写化学反应方程式_______。
能发生反应生成一种含五元环的化合物,请书写化学反应方程式_______。
如图杠杆AB两端分别挂着体积相同质量相同的空心铁球和空心铜球。调节杠杆使其保持平衡,一段时间后小心加入浓CuSO4溶液,回答下列有关问题(不考虑铁丝反应和两球的浮力变化)
(1)若杠杆为绝缘体,则A端_____(填“高”或“低”),发生反应的离子方程式___________。
(2)若杠杆为导体,则A端______(同上),在此过程中铁丝、杠杆、小球、CuSO4溶液构成了原电池,电极反应分别是,
正极:________________________,
负极:___________________________________。
(3)若杠杆为导体,一段时间通过杠杆电子数为0.1NA,则俩球质量相差g。
某学生为了探究锌与盐酸反应过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
| 时间(min) |
1 |
2 |
3 |
4 |
5 |
| 氢气体积(mL) |
50 |
120 |
232 |
290 |
310 |
(1)哪一时间段(指0~1、1~2、2~3、3~4、4~5 min)反应速率最大 ,原因是。
(2)哪一段时段的反应速率最小,原因是 。
(3)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列溶液:
A.Na2CO3溶液 B.NaCl溶液 C.NaNO3溶液 D.CuSO4溶液
你认为可行的是。
A、B、C、D、E、F六种短周期元素,原子序数依次增大。A、E同主族,且E元素原子的核外电子数是A元素原子核内质子数的两倍。B、C两元素原子的最外层电子数之和等于D元素原子的最外层电子数,C、D两元素原子最外层电子数之和等于F元素原子的最外层电子数。D元素原子最外层电子数是次外层电子数的一半。回答下列问题:
(1)写出E、F形成化合物所含化学键的类型;A元素在周期表中的位置是
(2)D、E、F的最高价氧化物的水化物酸性强弱顺序(用化学式表示)
(3)写出C、E对应的最高价氧化物的水化物相互反应的化学方程式为:
(4)C、D的氧化物与分别与B的氢氧化物反应的离子方程式:、