工业上“固定”和利用CO2能有效地减轻“温室”效应,可用CO2生产燃料甲醇:
CO2(g)+3H2(g)  CH3OH(g)+H2O(g) △H=-49.0 kJ·mol-1
CH3OH(g)+H2O(g) △H=-49.0 kJ·mol-1
(1)在相同温度和容积不变时,能说明该反应已达平衡状态的是 。
| A.n(CO2)∶n(H2)∶n(CH3OH)∶n(H2O)=1∶3∶1∶1 |
| B.容器内压强保持不变 |
| C.H2的消耗速率与CH3OH的消耗速率之比为3∶1 |
| D.容器内的密度保持不变 |
(2)一定温度下,将6 mol CO2和8 mol H2充入2L的密闭容器中,测得H2的物质的量随时间变化如图所示(实线)。图中数据a(1,6)代表的意思是:在1 min时H2的物质的量是6 mol。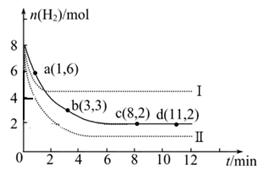
①a点正反应速率 逆反应速率(填“大于”、“等于”或“小于”),在1~3min内的平均反应速率v(H2)= 。
②仅改变某一实验条件时,测得H2的物质的量随时间变化如图中虚线所示,曲线I对应的实验条件改变是 ,曲线II对应的实验条件改变是 。
(3)甲醇可用于制作燃料电池,若电解质溶液为酸性,负极的电极反应式为: 。
(14分)某小组同学欲探究NH3与O2反应的反应过程,按下列装置进行实验。
(1)A、B装置中可选药品:浓氨水、H2O2、CaO、CaCO3、MnO2、浓盐酸、蒸馏水。
①则A装置中发生反应的化学方程式为_____________________________;B装置中锥形瓶中盛放的药品是______。
②E装置中氨气被催化氧化生成一氧化氮时的化学方程式为_______________。
③F装置中可以看到有红棕色气体和白烟生成,红棕色气体是__________(填化学式,下同),白烟的成分____________。
(2)另一小组的同学撤掉A、C装置,只用剩余装置来完成此实验,B装置中分液漏斗盛放的是浓氨水,那么B装置中的锥形瓶中盛放的固体药品是_____________。
(3)工业上制取的浓硝酸往往呈黄色,该小组成员设计实验探究硝酸呈黄色的原因,提出如下假设,请你完成假设二。
假设一:可能含有Fe3+;假设二:可能含有_____;假设三:可能含有上述两种微粒。检验是否含有Fe3+的方法是:取少量样品于试管中,加水稀释,__________________________(补充操作步骤、现象和结论)。
(4)工业上用氨、氧气和水为原料制取硝酸铵,如果用17吨氨气,最多可制取_______吨硝酸铵 (硝酸铵的相对分子质量为80)。
(12分)根据下图所示的关系,确定A、B、C、D、E、F的化学式,并写有关方程式。
(1)已知A为单质,则A为(填化学式,下同),E为。
(2)D→E的化学方程式为___________________________________。
(3)取少量C溶于水,加入酸化的硝酸银溶液,有白色沉淀生成,则A→C的化学方程式为_____________________________。
(4)某学习小组设计如下装置进行相关实验:
①打开活塞b,向溶液B中逐滴加入少量溴水,关闭活塞b;
②打开活塞a,向容器中滴入足量的亚硫酸。
按要求回答下列问题:
①滴入溴水时,溶液的颜色变为棕黄色,该反应的离子方程式为________。
②滴入亚硫酸时,溶液由棕黄色变为浅绿色,该反应的离子方程式为______。
③由此可知,B中的阳离子、Br-、H2SO3还原性由强到弱的顺序是___________(B中的阳离子用离子符号表示)。
(7分)下图是用废铜料(铁、铜混合物)来生产胆矾(CuSO4·5H2O)的过程,请根据图示回答下列问题。
(1)试剂X是___________(填名称)。
(2)途径Ⅱ的化学方程式为____________________________________。
(3)有关途径Ⅰ和途径Ⅱ的说法正确是___________(填编号)
a.途径Ⅰ的操作步骤比途径Ⅱ多,因此采取途径Ⅱ更合理
b.途径Ⅰ相比途径Ⅱ节省原料,且不产生污染
c.相同质量的单质A完全反应生成硫酸铜的量与途径无关
d.每生成1mol B,消耗1mol氧化剂,转移2mol电子
(4)称取25g胆矾,加热冷却后称量固体的质量减少了7.2g,则所得固体的化学式为___________。
(9分)“三酸两碱”是重要的化工原料,其中的“两碱”为氢氧化钠和碳酸钠。
(1)氢氧化钠不能保存在带玻璃塞的玻璃瓶中的原因是________________________。
(2)实验室配制100mL 1mol/L氢氧化钠溶液时,下列操作会导致浓度偏低的是_____
a.定容时仰视刻度线
b.容量瓶洗涤后没有干燥就直接用于溶液的配制
c.氢氧化钠溶解后没有冷却至室温,就将溶液转移到容量瓶中
d.定容摇匀后,发现液面低于刻度线,又加水使液面与刻度线相平
(3)将足量二氧化碳通入氢氧化钠溶液中的离子方程式为_________________。
(4)向碳酸钠溶液中逐滴加入稀盐酸至过量,碳酸氢根离子浓度变化趋势是_______;碳酸钠溶液中混有少量碳酸氢钠,可用氢氧化钠来除杂,反应的离子方程式为_______。
(6分)下表为各物质中所含有的少量杂质,在空格处填写除杂所用试剂和操作方法。
| 序号 |
物质 |
杂质 |
除杂质试剂 |
操作方法 |
| ① |
Fe(OH)3胶体[ |
Na+、Cl- |
水 |
|
| ② |
FeSO4溶液 |
CuSO4 |
||
| ③ |
CO2 |
HCl |
洗气 |
|
| ④ |
NaCl溶液 |
I2 |