(1)已知在一定条件下的反应4HCl+O2=2Cl2+2H2O中,有4mol HCl被氧化时,放出120kJ的热量,且有图1所示信息,则断开1mol H﹣O 键与断开 1mol H﹣Cl 键所需能量相差为 KJ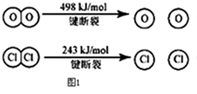
(2)科学家通过X射线探明,NaCl、KCl、MgO、CaO晶体结构相似,其中三种晶体的晶格能数据如下表:
| 晶体 |
NaCl |
KCl |
CaO |
| 晶格能/(kJ•mol﹣1) |
786 |
715 |
3401 |
四种晶体NaCl、KCl、MgO、CaO熔点由高到低的顺序是 .
(3)已知AlCl3熔点190℃,沸点183℃,结构如图2所示:则AlCl3晶体内含有的作用力有 .
A.离子键
B.共价键
C.金属键
D.配位键
E.范德华力
F.氢键
(4)氯和钾与不同价态的铜可生成两种化合物,这两种化合物中的阴离子均为无限长链结构(如图3),a位置上Cl原子的杂化轨道类型为 ,已知其中一种化合物的化学式为KCuCl3,另一种的化学式为 .
(方程式每空2分,其余每空1分,共21分。)氧化还原反应和离子反应是高一所学过的重要化学反应类型,仔细思考回答下列问题:
(Ⅰ)下列一组有水参与的反应:
①2Na + 2H2O =" 2NaOH" + H2↑
②2Na2O2 + 2H2O =" 4NaOH" + O2↑
③Na2O+ H2O ="2NaOH"
④3Fe+4H2O Fe3O4+4H2
Fe3O4+4H2
⑤2H2O 2H2↑+ O2↑
2H2↑+ O2↑
⑥2F2 + 2H2O =" 4HF" + O2
(1)其中不属于氧化还原反应的是(填编号)
(2)在这些氧化还原反应中,水只作氧化剂的反应是(填编号)
水只作还原剂的反应是(填编号)水既作氧化剂,又作还原剂是(填编号)
水既不作氧化剂,又不作还原剂是(填编号)
(3)根据你的理解,氧化还原反应的实质是()
| A.分子中的原子重新组合 | B.氧元素的得失 |
| C.电子的得失或共用电子对的偏移 | D.化合价的改变 |
(4)请你运用所学知识分析3NO2+H2O = 2HNO3+NO是否属于氧化还原反应?(填“是”或“不是”),若是,这个反应的氧化剂是,还原剂是。
(Ⅱ)写出下列反应的离子方程式:
①往氯化铁溶液加入铁粉:
②过量二氧化碳通入澄清石灰水:
③往氯化铝溶液中加入足量的NaOH溶液:
(Ⅲ)写出下列反应的化学方程式:
①二氧化硫发生催化氧化反应:
②氯气与氢氧化钠溶液反应:
③铜片与稀硝酸的反应:
(12分)湄潭中学某化学兴趣小组利用铁锈(Fe2O3)做了系列实验,物质间关系图如下。根据所学知识回答相关问题: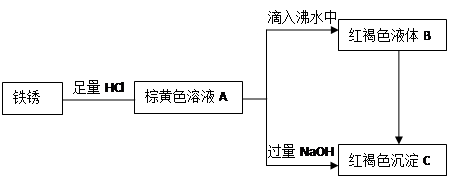
(1)写出A 、B、C三种物质的名称:
ABC
(2)写出由A滴入沸水中制备B的离子方程式:
(3)兴趣小组讨论了多种使B转换为C的方法,请写出你认为可行的一种方法:
(4)下列说法正确的有(填序号):
①B转换为C的过程发生了化学反应
②由A制备B时,加热越久越好
③物质B具有丁达尔效应
④把B、C的混合物过滤,滤液无色透明
⑤整个系列反应,都不涉及氧化还原反应
苯甲酸甲酯( )是一种重要的工业使用的有机溶剂。分析下面的框图关系,然后回答问题:
)是一种重要的工业使用的有机溶剂。分析下面的框图关系,然后回答问题:
已知以下信息:
①有机化合物甲的结构:
②有机化合物乙的结构:
③有机化合物丙的分子式为C7H8O,熔融状态的丙能与钠反应放出氢气,且能够与乙酸发生酯化反应;
④苯在无水AlCl3的作用下与卤代烃、烯烃发生反应,可以在苯环上增加烷基。
(1)乙中含氧官能团的名称 。
(2)甲、乙、丙三种有机物中与苯甲酸甲酯是同分异构体的是 ,在加热条件下能够与新制氢氧化铜悬浊液反应生成砖红色沉淀的是 ,与NaOH溶液加热消耗NaOH最多的是 。
(3)写出C的结构简式: 。
(4)丙生成甲的反应类型与 (选填序号)的反应类型相同。
a.反应I b.反应Ⅱ c.反应Ⅲ d.反应Ⅳ
(5)写出B生成丙的化学方程式: 。
工业上利用CO和水蒸气在一定条件下发生反应制取氢气:
CO(g)+H2O(g)  CO2(g)+H2(g)△H=-41 kJ/mol
CO2(g)+H2(g)△H=-41 kJ/mol
某小组研究在相同温度下该反应过程中的能量变化。他们分别在体积均为VL的两个恒温恒容密闭容器中加入一定量的反应物,使其在相同温度下发生反应。相关数据如下:
| 容器编号 |
起始时各物质物质的量/mol |
达到平衡的时间/min |
达平衡时体系能量的变化/kJ |
||||
| CO |
H2O |
CO2 |
H2 |
||||
| ① |
1 |
4 |
0 |
0 |
t1 |
放出热量:32.8 kJ |
|
| ② |
2 |
8 |
0 |
0 |
t2 |
放出热量:Q |
|
(1)该反应过程中,反应物分子化学键断裂时所吸收的总能量(填“大于”、“小于”或“等于”)生成物分子化学键形成时所释放的总能量。
(2)容器①中反应达平衡时,CO的转化率为%。
(3)计算容器②中反应的平衡常数K=。
(4)下列叙述正确的是 (填字母序号)。
a.平衡时,两容器中H2的体积分数相等
b.容器②中反应达平衡状态时,Q > 65.6 kJ
c.反应开始时,两容器中反应的化学反应速率相等
d.容器①中,反应的化学反应速率为:
(5)已知:2H2 (g) + O2 (g) ="=" 2H2O (g)ΔH=-484 kJ/mol,写出CO完全燃烧生成CO2的热化学方程式:。
(6)容器①中反应进行到t min时,测得混合气体中CO2的物质的量为0.6 mol。若用
200 mL 5 mol/L的NaOH溶液将其完全吸收,反应的离子方程式为(用一个离子方程式表示)。
A、B、C、D、E为中学常见的五种物质,均含元素Y,有的还可能含有元素X、Z,元素X、Y、Z的原子序数依次递增。
①元素Y在A、B、C、D、E中所呈现的化合价依次递增,其中只有B为单质;
②常温下将气体D通入水中发生反应,生成C和E;
③工业上以A、空气和水为原料,通过催化氧化法制取E。
请回答以下问题:
(1)B的电子式为:______,A的结构式为__________,A分子的空间构型是_______;
(2)写出②中涉及反应的化学方程式_____________________________________。
(3)由B反应生成1 molA放出的热量为46.2kJ,写出该反应的热化学方程式,并注明反应条件____________________________________________________________________。
(4)工业上,若输送Cl2的管道漏气,用A进行检验时可观察到大量白烟,同时有B生成,写出有关反应的化学方程式_______________________________________,生成的大量白烟属于_______化合物。