下图是实验室制备氯气并进行一系列相关实验的装置(夹持设备和A中加热装置已省略)。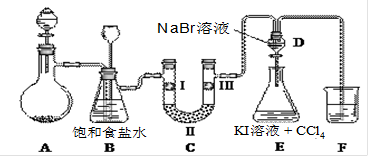
(1)制备氯气选用的药品为:二氧化锰和浓盐酸,相关反应的化学方程式为: 。
(2)装置B中饱和食盐水的作用是 ;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象 。
(3)装置F烧杯中盛放的试剂是 ,其中发生反应的离子方程式是 。
(4)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III依次放入 。
| 选项 |
I |
II |
III |
| A |
干燥的有色布条 |
碱石灰 |
湿润的有色布条 |
| B |
干燥的有色布条 |
硅胶 |
湿润的有色布条 |
| C |
湿润的有色布条 |
浓硫酸 |
干燥的有色布条 |
| D |
湿润的有色布条 |
无水氯化钙 |
干燥的有色布条 |
(5)设计装置D、E的目的是比较Cl2、Br2、I2的氧化性强弱。当向D中缓缓通入足量氯气时,可以看到无色溶液逐渐变为红棕色,说明Cl2的氧化性大于Br2。打开活塞,将装置D中少量溶液加入装置E中,振荡。观察到的现象是 。该现象 (填“能”或“不能”)说明Br2的氧化性强于I2,原因是 。
某学生实验兴趣小组拟用图1装置来完成“NaHCO3和NaCl混合物中NaHCO3含量的测定”的实验。
图1
(1)各仪器接口连接顺序是_________________(用接口字母填写)。
(2)该装置连接好而未装药品前,检验气密性的操作是_________________________。
(3)甲同学认为上述方法误差较大,提出如下改进措施,你认为可行的有______。(填序号)
| A.在滴入盐酸之前,应排净装置内的CO2气体 |
| B.在装置①中稀盐酸换成稀硫酸,装置②中水换成饱和NaHCO3溶液 |
| C.在装置②中水换成饱和Na2CO3溶液 |
| D.滴加盐酸不宜过快 |
(4)乙同学认为在装置②③之间的导管内会积存水,使测定结果不准,从而改用图2装置。假定滴定管起始读数为V1mL,终了读数为V2mL,而注射器测定排出的气体为V3mL(标准状况下),混合物样品质量为m g,则原混合物中NaHCO3的质量分数的表达式为_______。
(用含V1、V2、V3、m的式子表示)。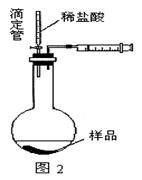
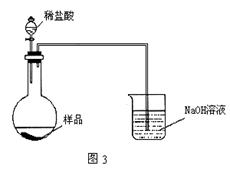
(5)丙同学改用图3装置,通过测定烧杯的质量。你认为乙、丙两同学的方案中,谁的方案更合理__________,理由是:_____________。
(6分) 溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下: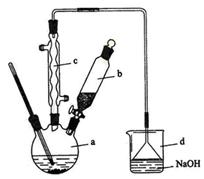
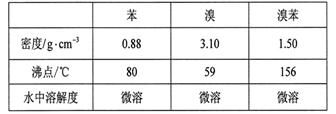
按下列合成步骤回答问题:
(1)在a中加入15 mL无水苯和少量铁屑。在b中小心加入4.0 mL液态溴。向a中滴入几滴溴,有白色烟雾产生,是因为生成了__________气体。继续滴加至液溴滴完。装置d的作用是____________________________________;
(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10 mL水,然后过滤除去未反应的铁屑;
②滤液依次用l0 mL水、8 mL l0%的NaOH溶液、10 mL水洗涤。NaOH溶液洗涤的作用是除去HBr和未反应的Br2;③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是;
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为______,要进一步提纯,下列操作中必须的是______(填入正确选项前的字母);
A重结晶 B过滤 C蒸馏 D萃取
(4)在该实验中,a的容积最适合的是______(填入正确选项前的字母)。
A 25 mL B 50 mL C 250 mL D 509 mL
某同学为了验证海带中含有碘,拟进行如下实验,请回答相关问题。
(1)第1步:灼烧。操作是将足量海带灼烧成灰烬。该过程中将使用到的硅酸盐质实验仪器除F外还有(填代号,限填2项)。
A.试管 B.瓷坩埚 C.坩埚钳 D.铁三脚架
E.泥三角 F.酒精灯 G.烧杯 H.量筒
(2)第2步:Iˉ溶液的获取。操作是。
(3)第3步:氧化。操作是依次加入合适的试剂。下列氧化剂最好选用(填代号)____________。
A.浓硫酸 B.新制氯水 C.KMnO4溶液 D.H2O2
理由是
(4)第4步:碘单质的检验。取少量第3步的溶液,滴加淀粉溶液,如果溶液显蓝色,则证明海带中含碘。
实验室采用不同的实验装置研究苯与液溴的反应类型并制取少量溴苯。试回答下列各小题:Ⅰ.若用图甲装置进行进行制备实验,回答下列问题: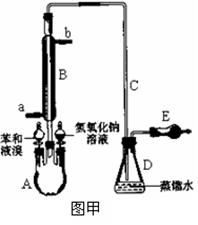
(1)写出下列仪器的名称:A、B。
(2)A中预先需加入的试剂是,E中需加入的试剂是。
(3)仪器B除导气外的作用是,进水口为(选填字母“a”或“b”)。
Ⅱ.若用图乙装置进行制备实验,回答下列问题: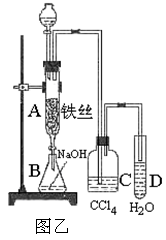
(1)C中盛放CCl4的作用是;
(2)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,写出有关的离子方程式 ,然后用仪器分离出溴苯(仍含有少量苯);
(3)反应完毕后,向试管D中滴加AgNO3溶液有 (填现象)生成,此现象说明这种获得溴苯的反应属于(填有机反应类型)。
实验室制备溴乙烷并进行溴乙烷的性质实验如下,试回答下列问题: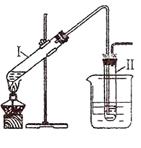
(Ⅰ)用右图所示的装置制取溴乙烷:
在试管I中依次加入2 mL 蒸馏水、4 mL浓硫酸、2 mL 95%的乙醇和3g溴化钠粉末,在试管Ⅱ中注入蒸馏水,在烧杯中注入冰水。加热试管I至微沸状态数分钟后,冷却。
(1)试管I中生成溴乙烷的化学反应方程式为:。
(2) 试管I中加入2 mL 的蒸馏水,其作用除溶解NaBr粉末和吸收HBr气体之外还有一个重要作用是_____。
(3)反应结束后,试管Ⅱ中粗制的C2H5Br呈棕黄色。为了除去粗产品中的杂质,可选择下列试剂中的 __________(填字母)
| A.NaOH溶液 | B.H2O | C.Na2SO3溶液 | D.CCl4 |
(4)下列几项实验步骤,可用于检验溴乙烷中溴元素,其正确的操作顺序是:取少量溴乙烷,然后____________________________(填代号)。
①加热;②加入AgNO3溶液;③加入稀HNO3酸化;④加入NaOH溶液;⑤冷却
(Ⅱ)溴乙烷的性质实验
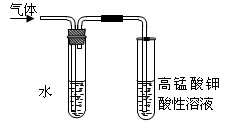
(5)在进行溴乙烷与NaOH乙醇溶液共热的性质实验时,把生成的气体通过右图所示的装置。用该装置进行实验的目的是检验乙烯的生成,该图中右边试管中的现象是;左边试管中水的作用是。