一定条件下反应2AB(g)  A2(g)+B2(g)达到平衡状态的标志是
A2(g)+B2(g)达到平衡状态的标志是
A.单位时间内生成n molA2,同时消耗2n molAB
B.容器内,3种气体AB、A2、B2共存
C.AB的消耗速率等于A2的消耗速率
D.容器中各组分的体积分数不随时间变化
工业废气中氮氧化物是主要的大气污染源之一。
已知:2NO2+2NaOH = NaNO3+NaNO2+H2O,NO2+NO+2NaOH = 2NaNO2+H2O。现有a mol NO2和bmol NO的混合气,若用足量的NaOH溶液将其完全吸收,则混合气中两种气体的物质的量必须满足的关系是:
| A.a=b/3 | B.2a=b | C.a≥b | D.a<b |
将少量SO2通入Fe2(SO4)3溶液中发生反应:SO2+2Fe3++2H2O = SO42-+2Fe2++4H+;然后再加入K2Cr2O7溶液,发生反应:Cr2O72-+6Fe2++14H+ =2Cr3++6Fe3++7H2O。下列判断正确的是
| A.还原性Cr3+> Fe2+> SO2 | B.氧化性Cr2O72-> SO2> Fe3+ |
| C.两个反应中Fe2(SO4)3均作还原剂 | D.Cr2O72-能将SO2氧化成SO42- |
美国科学家宣布发现了铝的“超级原子”结构——Al13和Al14,已知这类“超级原子”最外层电子数之和为40个时处于相对稳定状态,下列说法中,正确的是
| A.Al14与盐酸反应的化学方程式可表示为:Al14+2HCl= Al14Cl2+H2↑ |
| B.Al13和Al14互为同位素 |
| C.Al13和Al14都具有较强的还原性,容易失去电子生成阳离子 |
| D.Al13超原子中Al原子间通过离子键结合 |
向四支试管中分别加入少量不同的无色溶液,再分别进行如下操作,结论正确的是
| 操作 |
现象 |
结论 |
|
| A |
滴加BaCl2溶液 |
生成白色沉淀 |
原溶液中有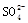 |
| B |
滴加氯水和CCl4,振荡、静置 |
下层溶液显橙红色 |
原溶液中有Br- |
| C |
用洁净铂丝蘸取溶液进行焰色反应 |
火焰呈黄色 |
原溶液中有Na+、无K+ |
| D |
滴加稀NaOH溶液,将湿润红色石蕊试纸置于试管口 |
试纸不变蓝 |
原溶液中无NH4+ |
下列反应的离子方程式正确的是
| A.用醋酸除去水垢:CaCO3 + 2H+=Ca2+ + H2O + CO2↑ |
| B.利用腐蚀法制作印刷线路板:Fe3+ + Cu = Fe2+ + Cu2+ |
| C.次氯酸钙溶液中通入过量二氧化硫:Ca2++2Cl0一+S02+H20=CaSO3↓+2HClO |
| D.等体积等物质的量浓度的氢氧化钡溶液与碳酸氢铵溶液混合: |
Ba2++20H-+NH4++HCO3-=BaC03↓+NH3·H2O+H20