现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
| A元素的核外电子数和电子层数相等 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能如下: I1=738 kJ·mol-1 I2=1451 kJ·mol-1 I3=7733 kJ·mol-1 I4=10540 kJ·mol-1 |
| D原子价电子层的p轨道半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |
(1)写出BA3的电子式:________。
(2)B元素基态原子中能量最高的电子,其电子云在空间有________个取向,原子轨道呈________形。
(3)某同学根据上述信息,推断C基态原子的核外电子排布图为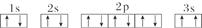
该同学所画的电子排布图违背了______________________________________。
(4)比较B和D的电负性_________>_______(填元素符号)
(5)G位于________族________区,该元素的核外电子排布式为________________________。
(6)检验F元素的方法是____________,请用原子结构的知识解释产生此现象的原因:_____。
(本题共12分)目前,碳族元素按原子序数增大,依次为:碳(C)、硅(Si)、锗(Ge)、锡(Sn)、铅(Pb)。请回答:
23.锗原子的最外层电子排布式:,锡原子的最外层电子云有种伸展方向; 单质锗具有__________(填字母)。
a.只有金属性
b.只有非金属性
c.既有金属性,又有非金属性
24.某同学根据反应:SiO2 + 2C Si + 2CO↑,得出结论:碳的非金属性强于硅的反应。请对此给予评价并说明理由:。
Si + 2CO↑,得出结论:碳的非金属性强于硅的反应。请对此给予评价并说明理由:。
25.常温下,在400mL稀氢氟酸中,投入一颗石英玻璃,2.5min后,溶液质量减少了11.22g。此时SiF4为气体,则这段时间内用HF表示该反应的平均化学反应速率为。
高温下,在容积固定的密闭容器中,用足量焦炭与一定量二氧化碳发生可逆的吸热反应生成了CO。回答26-27题:
26.下列选项中,一定符合反应达到化学平衡时情况的选项是。
a.压缩体积达到新平衡时,CO的浓度增大的倍数比CO2的浓度增大的倍数更大
b.速率关系:2v(CO2)= v(CO)
c.转移电子数随温度升高而增多
d.气体密度随着焦炭的增加而增大
27.达到化学平衡之后,保持其他条件不变,移走少量CO,达到新的平衡时,下列选项中,增大的是(填选项编号)。
A.CO2和CO浓度比b.混合气体的密度
c.转化率d.CO的体积分数
【化学选修3-物质结构与性质】X、Y、Z、W、Q五种前四周期元素,原子序数依次增大.已知X、Y、Z、W均为非金属元素,XW2分子与Y3为等电子体,元素W的原子序数等于元素Z的原子序数加8,Q的最外层电子数为2,次外层电子数等于Y和W2 -最外层电子数之和,根据以上信息回答下列问题:
(1)上述五种元素中电负性最大的是____(填元素符号,下同),Y的第一电离能大于Z的第一电离能原因。
(2)XW2的电子式为。Y3的分子构型为。
(3)Q的价电子排布式为。
(4)下列关于WZ2结构的说法正确的是。
a.WZ2直线形非极性分子
c.WZ2中w为sp3杂化
b.WZ2直线形极性分子
d.WZ2中W为sp2杂化
(5)d-QW的晶胞是立方体,用X射线衍射法测得该晶体晶胞边长a=520.0pm,26℃测得该晶体的密度为4.1g/cm3,请列式计算一个晶胞中含有的Q、W离子数。(5.23=140.6)
(6)d-QW的晶胞的一个侧面的投影图如图所示,与Q离子距离最近且距离相等的W离子构成的几何图形是________________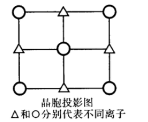
SiCl4在室温下为无色液体,易挥发,有强烈的刺激性.把SiCl4先转化为SiHCl3,再经氢气还原生成高纯硅.
(1)高温条件下,SiHCl3与氢气反应的方程式为:。
(2)已知:
(ⅰ)Si(S)+4HCl(g)=SiCl4(g)+2H2(g) △H=-241KJ.mol-1
(ⅱ)Si(S)+3HCl(g)=SiHCl3(g)+H2(g) △H=-210KJ.mol-1
则SiCl4转化为SiHCl3的反应(ⅲ):3SiCl4(g)+2H2(g)+Si(S)==4SiHCl3(g) △H=______。
(3)力研究反应(iii)的最适宜反应温度,下图为四氯化碳的转化率随温度的变化曲线:由图可知该反应最适宜的温度为,四氯化碳的转化率随温度升高而增大的原因为____。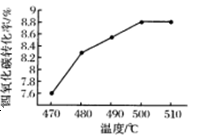
(4)一定条件下,在2L恒容密闭容器中发生反应(ⅲ),6h后达到平衡,H2与SiHCl3的物质的量浓度分别为1mol.L-1和0.2 mol.L-1
①从反应开始到平衡,v(SiCl4)=___________。
②该反应的平衡常数表达式为K=,温度升高,K值(填“”增大”、“减小”或“不变”)。
③原容器中,通入H2的体积(标准状况下)为。
④若平衡后再向容器中充人与起始时等量的SiCl4和H2(假设Si足量),当反应再次达到平衡时,与原平衡相比较,H2的体积分数将(填“增大”、“减小”或“不变”).
⑤平衡后,将容器的体积压缩为1L,再次达到平衡时,H2的物质的量浓度范围为。
将废旧锌锰电池处理得到含锰混合物,现以含锰混合物为原料制备锰锌铁氧体的主要流程如图l所示: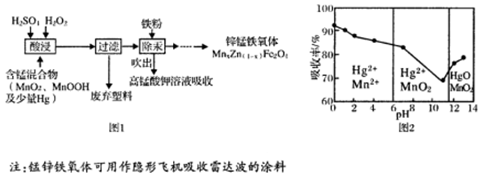
请回答下列问题:
(1)MnOOH中,锰元素的化合价为____。
(2)碱性锌锰干电池的电解质为KOH,Mn02参与的电板反应方程式为。
(3)酸浸时,MnO2与H2SO4、H2O2反应的离子方程式为。
(4)在不同pH下,KMnO4溶液对Hg的吸收率及主要产物如图2所示:
①pH对Hg吸收率的影响规律是。
②在强酸性环境下Hg的吸收率高的原因可能是。
(5)锰回收新方法:向含锰混合物加入一定量的稀硫酸、稀草酸,并不断搅拌至无气泡为止,其主要反应为:2MnOOH+MnO2+2H2C2O4+3H2SO4=3MnSO4+4CO2↑+6H2O
①当1molMnO2参加反应时,共有_____mol电子发生转移。
②MnOOH与浓盐酸在加热条件下也可发生反应,试写出其反应的化学方程式:_________________。
③已知:Ksp(MnCO3)=2.3×10-11、Ksp(Mn(OH)2))=2.1×10-13,欲制备MnCO3,选用的加料方式是______(填字母),原因是___________________________________。
a.将MnSO4溶液与Na2CO3溶液同时加入到反应容器中
b.将MnSO4溶液缓慢加入到盛有Na2CO3溶液的反应容器中
c.将Na2CO3溶液缓慢加入到盛有MnSO4溶液的反应容器中
d.以上三种方法都无法制得MnCO3
【化学---物质结构与性质】物质结构决定物质的性质,物质的性质反映物质结构。
(1)BCl3、NCl3发生水解反应化学方程式如下:
BCl3+ 3 H2O = B(OH)3 + 3 HCl
NCl3+ 3 H2O = NH3 +3 HClO
分析上述反应,判断B、N、Cl三种元素的电负性由大到小的顺序是____________________。上述反应所含的微粒中,呈三角锥形的是_____________(填化学式)。
(2)BN是一种新型无机非金属材料,熔点很高、硬度很大,晶胞结构如图所示。BN晶体中存在的作用力有____(填字母编号)。
A.σ键B.π键C.配位键D.分子间作用力
(3)B(OH)3晶体结构如图所示。晶体中B原子的轨道杂化方式是______________;B(OH)3可能具有的性质是_______(填字母编号)。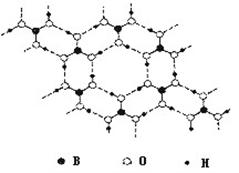
A.熔化状态下能导电B.熔点很高
C.能形成[B(OH)4]—D.硬度很大
(4)还原铁粉可作为合成氨的触媒。基态Fe原子的核外有________个未成对电子。从原子结构的角度分析,二价铁易被氧化为三价铁的原因是___________________________。