电子表所用的纽扣电池的两极材料为锌和氧化银,电解质溶液为KOH溶液,其电极反应式是: 。
。
总反应式为: 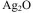
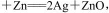 ,下列说法正确的是
,下列说法正确的是
| A.Zn为正极, Ag2O为负极 |
| B.电解质溶液中, OH-移向Ag2O极 |
| C.原电池工作时,正极区溶液pH值增大 |
| D.原电池工作时,负极区溶液pH值增大 |
有200 mL MgCl2、AlCl3的混合液,其中c(Mg2+)="0.2" mol·L-1,c(Cl-)为13 mol·L-1,要使Mg2+转化为沉淀分离出来,至少需加4 mol·L-1 NaOH溶液的体积为()
| A.40 ml | B.72 mL | C.80 mL | D.128 mL |
现有NaCl、Na2S、NaAlO2、NaHCO3和AgNO3五种无色透明溶液,选用一种试剂可以将它们区别开来,这种试剂是( )
| A.HNO3 | B.BaCl2 | C.HCl | D.NaOH |
洪涝地区欲将河水转化为可饮用水,下列处理过程中较合理的顺序是()
①化学沉降(用明矾)②消毒杀菌(用漂白粉)③自然沉降④加热煮沸
| A.②①④③ | B.③②①④ | C.③①②④ | D.③①④② |
下列反应的离子方程式,书写正确的是 ( )
A.铝溶解在NaOH溶液中2Al+2OH-+2H2O====2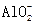 +3H2↑ +3H2↑ |
| B.氨水滴入AlCl3溶液中Al3++3OH-=====Al(OH)3↓ |
| C.MgO溶于稀HCl中O2-+2H+====H2O |
| D.Al(OH)3溶于稀H2SO4中OH-+H+====H2O |
甲、乙、丙、丁分别是Al2(SO4)3、FeSO4、NaOH、BaCl2四种物质中的一种,若将丁溶液滴入乙溶液中,发现有白色沉淀生成,继续滴加则沉淀消失,将丁溶液滴入甲溶液时,无明显现象发生,据此可推断丙物质是( )
| A.Al2(SO4)3 | B.NaOH |
| C.BaCl2 | D.FeSO4 |