在25℃时,冰醋酸加水稀释过程中溶液的导电能力变化曲线如图所示,请回答: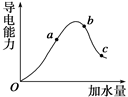
(1)O点为什么不导电 。
(2)a、b、c三点醋酸的电离度最大的是 ___(填“a”、“b”或“c”)。
(3)a、b、c三点的c(H+)由大到小的顺序是____________。
(4)在25℃时,已知c点溶液中pH="5," 则溶液中的c(OH-)= 。
(5)若使c点溶液中的c(CH3COO-)增大,不可以采取下列措施中的________ (填序号)。
| A.加热 | B.加水 | C.加NaOH固体 | D.加入锌粒 |
(6)随溶液的稀释,下列各项中始终保持增大趋势的是________(填序号)。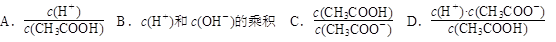
下列说法正确的是
| A.将明矾加入海水中静置过滤是海水淡化的方法之一 |
| B.海水晒盐的过程发生复分解反应 |
| C.海水中提取镁的过程不涉及氧化还原反应 |
| D.从海水中提取铀等微量元素是海水资源综合利用研究方向之一 |
已知核电荷数均小于18的X、Y、Z、W四种元素原子的电子层数相同,而原子半径依次增大,则下列物质中酸性最强的是
| A.HXO4 | B.H2YO4 | C.H3ZO4 | D.H4WO4 |
某元素R的最高价氧化物的水化物分子式是HnRO2 n-2,则在气态氢化物中R元素的化合价是
| A.3n-10 | B.12-3n | C.3n-4 | D.3n-12 |
下列粒子半径之比小于1的是
| A.r (Na+)/ r (Na) | B.r (Cl-)/ r (Cl) | C.r (Na)/ r (Mg) | D.r (Ca)/ r (Mg) |
已知某粒子 ,则元素R的原子序数是
,则元素R的原子序数是
| A.Z | B.A-Z | C.Z-n | D.Z+n |