填写计算结果:
(1)含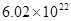 个分子的CO中,
个分子的CO中, 。
。
(2)
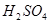 的
的 = 。
= 。
(3)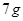
 在标准状况下的
在标准状况下的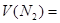 。
。
(4)5L
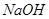 溶液中所含
溶液中所含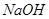 的
的 。
。
(5) 某二价金属氯化物(
某二价金属氯化物(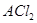 )中含有
)中含有 ,则A的相对原子质量= 。
,则A的相对原子质量= 。
元素周期表的形式多种多样,下图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表,思考扇形元素周期表的填充规律,并回答下列问题:
(1)D元素位于第周期第族。
(2)元素B、G、J、K、D的原子半径由大到小的顺序是(用元素符号表示)。
(3)K、G两种元素的最高价氧化物对应的水化物能发生反应,请写出该反应的化学方程式:。
(4)DA3、CE2、AK三种分子中,分子内所有原子都达到8电子稳定结构的分子为:(用化学式表示)。
已知拆开1 mol H—H键、1 mol I—I、1 mol H—I键分别需要吸收的能量为436kJ、151k J、299k J。则由氢气和单质碘反应生成1 mol HI需要(填“放出”或“吸收”)k J的热量。
下表为元素周期表中的一部分,列出了10种元素在元素周期表中的位置。试用元素符号、离子符号或化学式回答下列问题。
| ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
|
| 第2周期 |
⑥ |
⑦ |
||||||
| 第3周期 |
① |
③ |
⑤ |
⑧ |
⑨ |
⑩ |
||
| 第4周期 |
② |
④ |
(1)10种元素中,化学性质最不活泼的是;(填元素符号)
(2)①③⑤三种元素最高价氧化物对应水化物中,碱性最强的是,(填化学式)该物质内部含有的化学键类型是和;
(3)元素⑦的氢化物的化学式为;该氢化物常温下和元素②的单质反应的化学方程式;
(4)③和⑨两元素形成化合物的电子式是;①和⑦两元素形成四核化合物的电子式是,该物质与CO2反应的化学方程式为;
(5)①和⑤最高价氧化物对应水化物相互反应的离子方程式为:
。
X、Y、Z三种元素的离子结构都和Ar具有相同的电子层排布。H2在X单质中燃烧,产生苍白色火焰;Y元素的气态氢化物是H2Y,其最高价氧化物中Y的质量分数为40%;Z元素和氮元素在同一族。
(1)根据以上条件,推断X,Y,Z(填写元素名称);
(2)写出它们的最高价氧化物的水化物的化学式X,Y,Z。
工业上用乙烯和氯气为原料合成聚氯乙烯(PVC)。已知次氯酸能跟乙烯发生加成反应:CH2=CH2+HClO→CH2(OH)CH2Cl。以乙烯为原料制取PVC等产品的转化关系如图所示。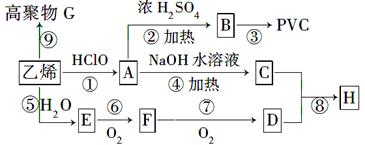
试回答下列问题:
(1)写出有机物B和G的结构简式:B____________,G_________;
(2)②、⑤、⑦的反应类型分别是_______________,_____________,________________;
(3)写出D的一种同分异构体的结构简式_____________;
(4)写出反应⑥的化学方程式__________________________________;
(5)E的核磁共振氢谱有三个峰,峰面积之比为:______________(由小到大)。
(6)写出C与D按物质的量之比为1∶2反应生成H的化学方程式:
______________________________________________________________;