某化学兴趣小组用100 mL 1 mol/L NaOH溶液完全吸收了a mol CO2后得到溶液A(液体体积无变化)。为了确定溶液A的溶质成分及a值,该兴趣小组的同学进行了如下实验。请帮助他们完成下列相应实验内容。
[提出假设]
假设Ⅰ:溶液A的溶质为NaOH、Na2CO3;
假设Ⅱ:溶液A的溶质为Na2CO3;
假设Ⅲ:溶液A的溶质为Na2CO3、NaHCO3;
假设Ⅳ:溶液A的溶质为 。
[实验过程]
(1)甲同学取少量溶液A于试管,再向试管中滴加几滴酚酞溶液,溶液A变红,由此得出假设I成立。
(2)乙同学分析后认为甲同学的实验结论有误。请用离子方程式说明乙同学的判断依据 ;他进一步提出,应先取少量溶液,向其中加入足量的 溶液,来检验溶液A是否含 ,结果加入检验溶液后观察到溶液A变浑浊。
(3)丙同学为了检验溶液A是否还含其它溶质,他将乙同学所得浑浊溶液进行过滤,并把滤液分为两份,向其中的一份加入稀硫酸,有无色气体生成,则假设 正确。
(4)为准确测定a值,丁同学取了10 mL 溶液A在锥形瓶中,用滴定管向其中加入某浓度的稀硫酸,记录加入硫酸的体积与生成气体的情况,并绘制成如图: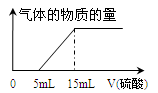
则a= ,所加硫酸的物质的量浓度为 。
粉末状试样A是由等物质的量的MgO和Fe2O3组成的混合物。进行如下实验:
①取适量A进行铝热反应,产物中有单质B生成;
②另取20 g A全部溶于0.15 L 6.0 mol/L盐酸中,得溶液C;
③将①中得到的单质B和溶液C反应,放出1.12 L(标准状况)气体,同时生成溶液D,还残留有固体物质B;
④用KSCN溶液检验时,溶液D不变色。
请回答:
(1)①中引发铝热反应的实验操作是_____________________________________,产物中的单质B是________________。
(2)②中所发生的各反应的化学方程式是_____________________________________。
(3)③中所发生的各反应的离子方程式是______________________________________。
(4)若溶液D的体积仍视为0.15 L,则该溶液中c(Mg2+)为________,c(Fe2+)为_______。
A、B、C、D四种化合物,其中A、C、D焰色反应均为黄色,而B的焰色反应为紫色,A、C和盐酸反应均得到D,将固体C加热可得到A,若在A的溶液中通入一种无色无味气体,又可制得C,若B的溶液滴加到硫酸亚铁溶液会先后出现白色沉淀→灰绿色沉淀→红褐色沉淀E。试推断
A:________、B:________、C:_________、D:_________、E:。
运用比较方法是化学科学中研究物质性质的基本方法之一,请运用比较法解答题目。过氧化钠几乎可与所有的常见气态非金属氧化物反应。如:2Na2O2+2CO2 2Na2CO3+O2↑,Na2O2+CO
2Na2CO3+O2↑,Na2O2+CO Na2CO3。
Na2CO3。
(1)试分别写出Na2O2与SO2、SO3反应的化学方程式:________、________。
现有A、B、C、D、E五种溶液,只知道它们的溶质是NaHCO3、Na2CO3、NaOH、HCl、Ca(HCO3)2。为了鉴别开来,各取少量进行如下实验:
(1)A与B混合无明显现象
(2)B与C(或D,或E)混合均有无色气体产生
(3)D与A(或E)混合均有白色沉淀产生
是根据以上现象,写出A~E各物质的名称:
A;B;C;D;E。