(12分)电化学技术在日常生活、化工生产、环境保护等方面都有重要研究和应用。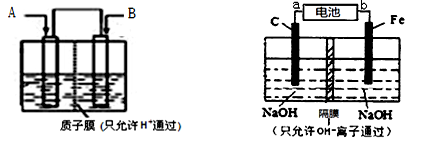
(1)有学者想以上左图所示装置将CO2转化为重要的化工原料甲醇,电解质为稀硫酸,特殊电极材料不参与反应。A为CO2,B为H2,电池总反应式为CO2+3H2=CH3OH+H2O,
①正极反应式为 ;
②反应时溶液中H+通过质子膜向 (填“左”或“右”)槽移动;
(2)高铁酸酸钠(Na2FeO4)是一种新型净水剂,用电解法可以直接制取高铁酸钠,电解装置上右图所示。
①a为电池 极(填“正”或“负”);
②阳极的电极反应式为 ;
③当制得99.6g高铁酸钠时,阳极区OH-的变化量为 mol;
④你认为高铁酸钠作为一种新型净水剂的理由可能是 。
A.高铁酸钠具有强氧化性,能消毒杀菌
B.高铁酸钠溶于水形成一种胶体,具有较强的吸附性
C.高铁酸钠在消毒杀菌时被还原生成Fe3+,水解产生氢氧化铁胶体能吸附悬浮杂质
现有部分短周期元素的性质或原子结构如下表:
| 元素编号 |
元素性质或原子结构 |
| T |
M层上有2对成对电子 |
| X |
最外层电子数是次外层电子数的2倍 |
| Y |
常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z |
元素最高正价是+7价 |
(1)元素T的原子最外层共有______种不同运动状态的电子。元素X的一种同位素可测定文物年代,这种同位素的符号是_________。
(2)元素Y与氢元素可形成离子YH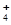 ,YH
,YH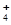 离子的结构式为。
离子的结构式为。
(3)元素Z与T相比,非金属性较强的是_______(填元素名称),下列表述中能证明这一事实的是________。
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
d.Z更易与H2化合
e.Z和T均可与铁化合,但Fe在与Z生成的化合物中价态更高
(4)写出两种由上述某两种元素组成的非极性分子的结构式
,。
已知A、B、C、D、E五种分子所含原子数目依次为1、2、3、4和6,且都含有18个电子。又知B、C和D是由两种元素的原子组成。请回答:
(1)组成A分子的元素在元素周期表中的位置是 ;
(2)B和C的分子式分别是_______和_______,C分子的立体构型呈_____形,属于_______分子(填“极性”或“非极性”);
(3)若向D的稀溶液中加入少量二氧化锰,有无色气体生成,则D的结构式是________,该反应的化学方程式为__________________;
(4)若将1mol E在氧气中完全燃烧,只生成1mol CO2和2mol H2O,则E是 (填名称)。E可以作为燃料电池的燃料,请写出以E为燃料,O2做氧化剂,KOH为电解质溶液组成的燃料电池的负极反应方程式 。
(1)把CoCl2溶于水后加氨水直到先生成的Co(OH)2沉淀又溶解后再加氨水,使生成2+,此时向溶液中通入空气,得到的产物中有一种其组成可用CoCl3·5NH3表示。把分离出CoCl3·5NH3溶于水后立即加硝酸银溶液,则析出AgCl沉淀。经测定,每1mol CoCl3·5NH3只生成2molAgCl。请写出表示此配合物结构的化学式:此配合物中的Co化合价为
(2)主族元素R的最高价氧化物R2O 4.7g溶于95.3g水中,所得溶液的质量分数为5.6%,R原子核中含有20个中子;主族元素Q,其单质与水剧烈反应放出O2,并能跟R形成典型离子化合物RQ。R的元素名称是_______,Q单质与水反应的化学方程式为______________。将4.7g R2O溶于_______g水中,可使每50个水分子中溶有1个R+离子。
X、Y、Z三种常见元素的单质,甲、乙是两种常见的化合物,相互间有如右图转化关系。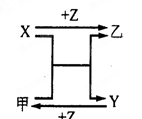
回答下列问题:
(1) 若X基态原子外围电子排布式为3s2,甲是由第二周期两种元素的原子构成的非极性气态分子, Y原子的基态轨道表示式为,乙的电子式为。
(2) 若X基态原子外围电子排布式为3s1,Y具有许多优越的性能,被称为未来金属,甲中共含有90个电子,则其分子式为,Y的电子排布式为。
(3) 若X、Y均为金属单质,X基态原子外围电子排布式为3s23p1,甲为具有磁性的黑色固体,则X与甲反应的化学方程式为:,Y原子基态电子排布式为。
用VSEPR模型和杂化轨道理论相关知识填表:
| 分子或离子 |
孤对电子对数 |
VSEPR模型名称 |
中心原子杂化轨道类型 |
分子或离子的立体构型名称 |
| CH4 |
0 |
正四面体形 |
sp3 |
正四面体形 |
| BeCl2 |
||||
| SO2 |
||||
| CH3+ |
||||
| SO42- |
||||
| NCl3 |