下图是实验室制取并收集Cl2的装置。A是Cl2发生装置,E是硬质玻璃管中装有细铁丝网;F为干燥的广口瓶,烧杯G为尾气吸收装置。
试回答:
(1)A中发生的化学反应方程式为 。
(2)C、D、G中各装的药品:C__________;D__________;G__________。
(3)E中的现象为 ;反应方程式为 。
(4)写出G中反应的离子方程式 。
(5)若将Cl2和SO2等物质的量混合漂白作用减弱,用化学方程式解释原因 。
实验室模拟合成氨和氨催化氧化的流程如下,气体混合的装置如图甲所示,合成氨的装置如图乙所示,氨吸收和氨氧化的装置如图丙所示。
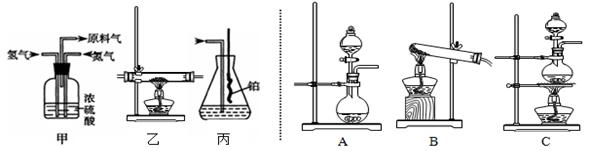
(1)已知实验室可用饱和亚硝酸钠(NaNO2)溶液与饱和氯化铵溶液经加热后反应制取氮气。则制取氮气的装置为_______(从上图A、B、C中选择,下同),制取氢气的装置为_______。
(2)甲装置的作用除了使气体充分混合外,还有①___________________、②_____________________。
(3)乙装置发生反应的化学方程式为_________________________。其中催化剂为Fe粉,它能否用Fe2O3代替?说明理由。___________________________________________________________。
(4)丙装置吸收一段时间氨气后,再通入空气,同时将经加热的铂丝插入到锥形瓶内,可观察到:有红棕色气体和白烟生成,请用化学方程式说明催化氧化后,产生以上现象的原因:___________________;__________________________,_________________________________。
(10分)锌与不同浓度的硫酸反应时,硫酸可以被还原为SO2,也可被还原为氢气。为了验证这一事实,某同学拟用下图装置进行实验(实验时压强为101 kPa,温度为0 ℃)。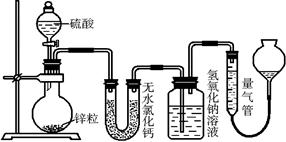
(1)若在烧瓶放入1.30 g锌粒,与c mol/L H2SO4反应,为保证实验结论的可靠,在洗气瓶中加入1 mol/L NaOH溶液的体积V≥______mL,量气管的适宜规格是__________ (选填“200 mL”、“400 mL”或“500 mL”)
(2)若1.30 g锌粒完全溶解,氢氧化钠洗气瓶增重1.28 g,则发生反应的化学方程式为:___________________________________________________________________
(3)若烧瓶中投入a g锌且完全反应,氢氧化钠洗气瓶增重b g,量气瓶中收集到V mL气体,则有:a/65 mol=b/64 mol+V/22400 mol,依据的原理是__________________。
(4)若在烧瓶中投入d g锌,加入一定量的c mol/L 浓硫酸V L,充分反应后锌有剩余,测得氢氧化钠洗气瓶增重m g,则整个实验过程产生的气体中,n(H2)/n(SO2)=____(用含字母的代数式表示)。
(14分)下表为元素周期表的一部分:(用元素符号或化学式填空)
| 族 周期 |
||||||||
| ① |
||||||||
| ② |
||||||||
| ③ |
④ |
⑤ |
⑥ |
(1)写出元素④在周期表中的位置______________。
(2)②、③、⑤的原子半径由大到小的顺序为_________________________。
(3)④、⑤、⑥的气态氢化物的稳定性由强到弱的顺序是_________________________。
(4)①、②、③、⑥中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:____________________。
Ⅱ.由上述部分元素组成的物质间,在一定条件下,可以发生下图所示的变化,其中A是一种淡黄色固体。请回答:
(1)写出固体A与液体X反应的离子方程式。
(2)气体Y是一种大气污染物,直接排放会形成酸雨。可用溶液B吸收,当B与Y物质的量之比为1:1且恰好完全反应时,所得溶液D的溶质为(填化学式)。
(3)写出气体C与气体Y反应的化学方程式。
Ⅰ.化学是一门以实验为基础的学科,下列实验操作描述中正确的是()
① 为使稀硫酸和锌制取氢气的速率加快,可向稀硫酸中加入用铜丝网包裹的锌粒
② 用托盘天平称取10. 4 g食盐时,将食盐放在右盘中的纸片上称量
③ 配制一定物质的量浓度的溶液时,容量瓶洗涤后未进行干燥,对实验结果无影响
④ 以酚酞作指示剂,用标准浓度的盐酸滴定NaOH溶液时,锥形瓶水洗后又用待测液润洗
⑤ 测定溶液的pH时,用洁净、干燥的玻璃棒蘸取待测溶液,点在试纸中部,待变色后与标准比色卡对照读数
⑥用标准浓度的盐酸滴定NaOH溶液时,滴定前仰视读数,滴定后俯视读数,这种操作将造成待测烧碱溶液浓度偏高
Ⅱ.某校化学兴趣小组采用酸碱中和滴定法测定学校新购入的烧碱的纯度(烧碱中含有不与酸反应的杂质),试根据实验回答。
(1)实验步骤为:①用托盘天平准确称量4.1g烧碱样品。
②将样品配成250ml待测液,需要的仪器除玻璃棒、量筒、烧杯外还需要的玻璃仪器有______________________。
③用________量取10.00ml待测液,注入锥形瓶中。
④在锥形瓶中滴入2~3滴________(填指示剂),用0.2010 mol/L的标准盐酸滴定待测烧碱溶液,滴定时左手旋转__式滴定管的玻璃活塞,右手不停地摇动锥形瓶,两眼注视___________,直到滴定终点。
(2)该小组测得下列数据
| 滴定次数 |
待测液体积/ml |
标准盐酸体积/ml |
|
| 滴定前读数/ml |
滴定后读数/ml |
||
| 第一次 |
10.00 |
0.20 |
22.90 |
| 第二次 |
10.00 |
0.50 |
20.40 |
| 第三次 |
10.00 |
4.00 |
24.10 |
| 第四次 |
10.00 |
0.00 |
20.00 |
根据上述数据,计算烧碱的纯度______________。
(8分) 50 mL 0.50 mol·L-1的盐酸与50 mL 0.55 mol·L-1NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热,完成下列问题: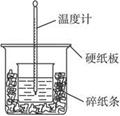
(1)从实验装置上看,图中尚缺少的一种玻璃用品是_____________。请指出装置中的另外错误是.
(2)烧杯间填满碎纸条的作用是___________。
(3)大烧杯上如不盖硬纸板,求得的中和热值___________(填“偏大”“偏小”“无影响”)。
(4)实验中改用60 mL 0.50 mol·L-1的盐酸跟60 mL 0.55 mol·L-1NaOH溶液进行上述实验相比,所放出的热量___________(填“相等”“不相等”),所求中和热___________(填“相等”“不相等”)。
(5)用相同浓度体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会_________________;用50 mL 0.50 mol·L-1NaOH溶液进行上述实验,测得的中和热的数值会___________(均填“偏大”“偏小”“无影响”)。