(15分)
I.从海水中可以提取氯、溴、碘等卤族元素。
(1)碘元素在周期表中的位置为_________________________。
(2)已知:X2(g)+H2(g)  2HX(g)(X2表示C12、Br2和12)。下图表示平定衡常数K与温度t的关系。
2HX(g)(X2表示C12、Br2和12)。下图表示平定衡常数K与温度t的关系。
①△H表示X2与H2反应的焓变,△H_______O。(填“>"、“<’’或‘‘=’’)
②曲线a表示的是________(填“C12”、“Br2"或“12’’)与H2反应时K与t的关系。
II.C12是一种重要的化工原料。
(3)液氯储存区贴有的说明卡如下(部分):
| 危险性 |
 |
| 储运要求 |
远离金属粉末、氨、烃类、醇更物质;设置氯气检测仪 |
| 泄漏处理 |
NaOH、NaHS03溶液吸收 |
| 包装 |
钢瓶 |
①用离子方程式表示“泄漏处理’’中NaHS03溶液的作用__________________。
②若液氯泄漏后遇到苯,在钢瓶表面氯与苯的反应明显加快,原因是__________________。
③氯气含量检测仪工作原理示意图如下:C12在Pt电极放电的电极反应式是_______________。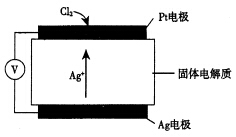
(4)质量标准要求液氯含水量(以1 g氯气含水的质量计)<0.4 mg,含水量超标会严重腐蚀钢瓶。液氯含水量的测定装置如下图所示: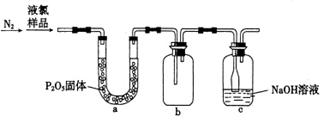
(已知:P205+3H20=2H3P04;C12与P205不反应。)
检测液氯的含水量,根据上图,需要测定的数据是_______________________________。
甲醛是一种重要的化工产品,可利用甲醇催化脱氢制备气态甲醛。甲醛与气态甲醇转化的能量关系如图所示:
(1)甲醇催化脱氢转化为甲醛的反应是 (填“吸热”或“放热”)反应.
(2)过程Ⅰ与过程Ⅱ的反应热是否相同? ,理由是 。
。
(3)合成甲醇的主要反应为:CO(g)+2H2(g) CH3OH(g)△H<0,其化学平衡常数K和温度T的关系如下表所示:
CH3OH(g)△H<0,其化学平衡常数K和温度T的关系如下表所示:
| T/℃ |
T1 |
T2 |
T3 |
| K |
1/1000 |
1/40 |
25 |
T1、T2、T3的大小关系为
X、Y、Z三种气体都是大气污染物,在工业上通常都用碱溶液吸。已知X是造成酸雨的主要物质;Y是一种单质,其水溶液具有漂白作用;Z是硝酸工业和汽车尾气中的有害物质之一,易溶于水。
(1)写出X、Y、Z的化学式:
X ; Y ; Z 。
(2)X能使湿润的红布条褪色,通过方法能使布条颜色复原。
(3)写出下列有关反应的化学方程式:
X在一定条件下与氧气反应。
Y与NaOH溶液反应。
Z与水反应。
在一固定容积的密闭容器中,保持一定条件下进行以下反应:X(气)+2Y(气)  3Z(气)。已知加入1 molX和3molY。达到平衡后,生成a mol Z。
3Z(气)。已知加入1 molX和3molY。达到平衡后,生成a mol Z。
(1)在相同实验条件下,若在同一容器中改为加入2 mol X和6 mol Y,达到平衡后,Z的物质的量为。
X和6 mol Y,达到平衡后,Z的物质的量为。
(2)在相同实验条件下,若在同一容器中改为加入0.5molX,则需加入mol Y,加入mol Z,才能使平衡时Z为0.9 a mol。
在密闭容器中进行可逆反应:CO (g)+NO2(g)  CO2 (g) + NO (g)(正反应为放热反应),达到平衡后,只改变其中一个条件,对平衡的影响是:(填“向左”、“向右”、“不移动”或颜色“变深”、“变浅”或“不变化”)
CO2 (g) + NO (g)(正反应为放热反应),达到平衡后,只改变其中一个条件,对平衡的影响是:(填“向左”、“向右”、“不移动”或颜色“变深”、“变浅”或“不变化”)
(1)增大容器的体积,平衡____________,反应混合物的颜色____________;
(2)通入CO2气体,平衡____________,反应混合物颜色_______________;
(3)升高温度,平衡_______________,反应混合物的颜色____________;
(4)加入一定量的N2,平衡____________,反应混合物的颜色___________;
(5)加入催化剂,平衡________________。
在某一化学反应中,反应物B的物质的量浓度在5 s内从2.0 mol·L-1变成
0.5 mol·L-1,在这5 s内B的化学反应速率为。